Молекулы фото из пластилина: Как слепить молекулы из пластилина.
Как слепить молекулы из пластилина.
Многие школьники не любят химию и считают ее скучным предметом. Многим этот предмет дается с трудом. Но ее изучение может быть интересным и познавательным, если подойти к процессу творчески и показать все наглядно.
Предлагаем вам подробное руководство по лепке молекул из пластилина.
Перед изготовлением молекул нам нужно заранее определиться с тем, какие химические формулы будем использовать. В нашем случае это этан, этилен, метилен. Нам понадобятся: пластилин контрастных цветов (в нашем случае – красный и синий) и немного зеленого пластилина, спички (зубочистки).
1. Из красного пластилина скатываем 4 шарика диаметром около 2 см (атомы углерода). Затем из синего пластилина скатываем 8 шариков поменьше, диаметром около сантиметра (атомы водорода).
2. Берем 1 красный шарик и вставляем в него 4 спички (или зубочистки)так, как показано на рисунке.
3. Берем 4 синих шарика и надеваем их на свободные концы вставленных в красный шарик спичек.
4. Повторяем шаг №3 и получаем две молекулы для следующего химического вещества.
5. Сделанные молекулы нужно соединить между собой спичкой для того, чтобы получилась молекула этана.
6. Также можно создать молекулу с двойной связью — этилен. Для этого, из каждой молекулы, полученной при выполнении шага № 3 вынимаем по 1 спичке с надетым на нее синим шариком и соединяем детали между собой двумя спичками.
7. Берем красный шарик и 2 синих и соединяем их между собой двумя спичками так, чтобы получилась цепочка: синий – 2 спички – красный – 2 спички – синий. У нас получилась еще одна молекула с двойной связью – метилен.
8. Берем оставшиеся шарики: красный и 2 синих и соединяем их спичками между собой как показано на рисунке. Затем скатываем из зеленого пластилина 2 маленьких шарика и прикрепляем к нашей молекуле. У нас получилась молекула с двумя отрицательно заряженными электронами.
Изучение химии станет интереснее, а у вашего ребенка появится интерес к предмету.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter
Молекула воды из пластилина: фото
[h3]
Молекула воды[/h3]
С водой связана вся жизнь человека – от самого зарождения и до смерти. Вода – это одно из самых первых веществ, которое начинает изучать маленький исследователь – в ванне, луже и даже на кухонном столе. Ее уникальные свойства испаряться, замерзать, таять (плавиться) привлекает умы деток постарше.
Но о том, почему так происходит и из чего состоит хорошо известная вода – узнается только в старших классах школы. Однако мы склонны считать, что не стоит ждать пока познавательный интерес к этому уникальному по своим свойствам веществу начнет угасать.
Моделируем молекулу из пластилина
Для того чтобы смоделировать молекулу воды потребуется пластилин двух цветов и спички.
Молекула воды состоит из атомов двух элементов – водорода и кислорода
.
В Периодической системе Д.И. Менделеева эти элементы расположены под номером 1 и 8. Этот номер называется порядковым. Ниже в этой же клеточке есть еще одно число (с несколькими цифрами после запятой) – это относительная атомная масса элемента.
[h3]
Кислорода:[/h3]
и
водорода:
Заметим, что масса получившихся «атомов» по сравнению с настоящими увеличена в 1000 000 000 000 000 000 000 000 (10 в 24 степени) раз.
По размеру получилось примерно, что атом кислорода «похож» со сливу, а атом водорода – на горошину.
В молекуле воды два атома водорода и один атом кислорода располагаются достаточно близко друг к другу, но под определенным углом. Если обозначить «центр» атома кислорода точкой, приложить к нему центральную метку транспортира, то атомы водорода будут находиться по отношению друг к другу под углом 104 градуса.
В итоге у нас получилась вот такая модель молекулы воды:
Модель клетки из пластилина | МОРЕ творческих идей для детей
Как сделать модель живой (животной) клетки из пластилина своими руками (тема «Строение клетки», 5 класс).
Модель клетки (строение клетки) из пластилина
Так как моя старшая дочь из-за плановой госпитализации некоторое время не посещала школу, пропущенные темы мы с ней изучали самостоятельно. «Строение клетки» — одна из таких тем. Я вспомнила, что сама когда-то делала в школу в качестве домашнего задания по биологии модель инфузории-туфельки из пластилина, которая так мне понравилось, что даже отдавать не хотелось.
Модель клетки дочка отнесла в школу. Оказалось, что это было домашним заданием, и другие дети тоже делали клетку из пластилина.
Как сделать модель живой (животной) клетки из пластилина
Для макета лучше всего подойдет не обычный пластилин, поделки из которого могут деформироваться от падения, от высокой температуры (например, от летнего зноя или под прямыми солнечными лучами) и т.д., а эластичная мягкая полимерная глина, застывающая на воздухе. Подробнее я писала о ней в статье «Легкая самозатвердевающая масса для лепки». Мы очень любим из нее лепить, но у нас она закончилась, поэтому в этот раз пришлось работать с простым пластилином.
Сделать модель живой животной клетки из пластилина можно несколькими способами (в статье использованы иллюстрации из учебника «Биология. Введение в биологию», 5 класс, авторы: А. А. Плешаков, Н. И. Сонин, 2014, художники: П. А. Жиличкин, А. В. Пряхин, М. Е. Адамов).
В. Пряхин, М. Е. Адамов).
1. Самая простая плоская модель клетки из пластилина на картоне
Самый простой способ изобразить схему строения клетки, на изготовление которого потребуется меньше всего времени, это слепить из пластилина клетку в соответствии с изображением из учебника.
Этапы работы
- Скатать из пластилина длинную тонкую колбаску и небольшой шарик. Шарик расплющить. Это детали, изображающие наружную мембрану и ядро.
- Приклеить детали на прямоугольный лист картона. Роль цитоплазмы будет играть поверхность картона внутри замкнутого контура (наружной мембраны).
- Сделать сноски и подписи.
2. Плоская модель живой клетки из пластилина
- Вырезать из плотного глянцевого картона основу овальной или слегка изогнутой формы.

- Приклеить детали, изображающие главные части клетки:
— наружную мембрану (сделать ее из скатанного колбаской пластилина)
— ядро (сделать его из расплющенного пластилинового шарика). - По желанию приклеить некоторые важные органоиды живой клетки: митохондрии, лизосомы.
- Подписи можно сделать прямо на картоне внутри клетки.
Этот же вариант модели клетки можно еще немного усложнить, если в начале работы на основе из картона тонким слоем размазать светлый пластилин (это будет цитоплазма).
3. Модель живой клетки из пластилина на пластике
Так как пластилин через некоторое время оставляет жирные пятна даже на глянцевом картоне, то модель клетки получится более долговечной, если сделать ее на основе из пластика. При использовании прозрачного пластика можно не покрывать основу пластилином. А сноски или надписи, сделанные не на самой модели, а на бумаге под ней, будут хорошо видны через прозрачный материал.
Модель мы делали на основе иллюстраций из пункта 5 «Живые клетки» первой части учебника.
Этапы работы
- Подготовить основу из прозрачного пластика. Это может быть пластик от упаковки различных товаров. Например, крышка от пластикового продуктового контейнера.
- Вырезать по краям пластика выемки.
- Сделать ядро: скатать шарик из коричневого пластилина, расплющить и приклеить на основу в центр или недалеко от центра. По желанию можно изобразить ядрышко, находящееся внутри ядра, из расплющенного маленького шарика более темного цвета.
- Сделать лизосомы: скатать маленькие шарики (4 штуки), приклеить их на основу.
- Сделать митохондрии: скатать шарики немного побольше, чем для лизосом, немного раскатать их как для колбаски, расплющить, приклеить на основу.
- По желанию сделать другие элементы животной клетки: эндоплазматическую сеть, аппарат Гольджи, центриоли и т.д.
- Сделать наружную мембрану: скатать из пластилина тонкую колбаску, немного ее расплющить и приклеить по контуру основы.
 Сразу сделать колбаску нужной длины сложно, но можно соединить друг с другом несколько коротких колбасок.
Сразу сделать колбаску нужной длины сложно, но можно соединить друг с другом несколько коротких колбасок. - Оформить работу в программе «Word»: сверху поместить заголовок «Строение клетки», в левом нижнем углу — информацию об ученике, выполнившем работу, сделать рамочку. Распечатать. Или написать это от руки. Затем приклеить этот лист на картон.
- Сделать сноски, подписи.
- Приклеить модель клетки в центр. Пластик очень хорошо держится на картоне, если приклеить его с помощью двусторонней клейкой ленты (скотча). На нашей модели кусочек двустороннего скотча размером с ядро под ним и расположен, поэтому его не видно.
- Поместить работу в файл — специальный прозрачный полиэтиленовый пакет для документов.
4. Объемная модель живой клетки из пластилина
- Для основы скатать из пластилина большой шарик, придать ему форму яйца и вырезать из него четверть.
- Для экономии пластилина можно сделать эту деталь из мягкой фольги, а затем облепить ее пластилином.
 Еще проще сделать эту деталь из пенопластового яйца для поделок.
Еще проще сделать эту деталь из пенопластового яйца для поделок. - Приклеить детали из пластилина (аналогично тому, как описано в предыдущей инструкции).
5. Модель живой клетки из соленого теста
Также можно сделать макет клетки из соленого теста (в этой статье рецепт соленого теста, который я использую).
- Соленое тесто раскатать скалкой в пласт толщиной около половины сантиметра.
- Вырезать из него основу для макета клетки.
- Приклеить основные детали.
- Оставить на сутки или двое в теплом месте для высыхания.
- Раскрасить красками.
Модели живых (животных и растительных) клеток своими руками
Напоследок небольшая галерея с фотографиями моделей клеток из кабинета биологии. Прошу прощения за качество фотографий — дочка делала их в школе телефоном, а там, где стоит шкаф с работами детей, плохое освещение.
А эта работа мне очень понравилась, потому что у меня тоже была идея сделать модель еще и из бумаги, в технике объемной аппликации.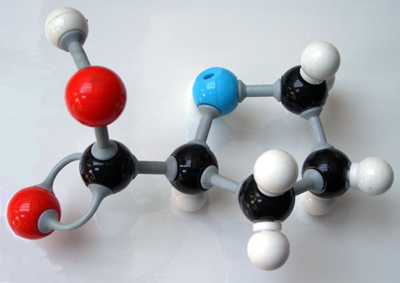 Модель клетки выполнена из бумаги в техниках рисования, аппликации и квиллинга.
Модель клетки выполнена из бумаги в техниках рисования, аппликации и квиллинга.
Предлагаю посмотреть другие статьи из рубрики «Школьные задания» или статьи о поделках из пластилина, массы для лепки, соленого теста и т.д.
© Юлия Валерьевна Шерстюк, https://moreidey.ru
Всего доброго! Если материалы сайта были Вам полезны, пожалуйста, поделитесь ссылкой на них в соцсетях — Вы очень поможете развитию сайта.
Размещение материалов сайта (изображений и текста) на других ресурсах без письменного разрешения автора запрещено и преследуется по закону.
Молекула воды и ее состояния. Эксперименты. — 3 ответов на Babyblog
Всем привет от нас с Сережей! Я реже появляюсь в блоге, но часто в инстаграме alinaland, заглядывайте!
В пятницу вечером мы с Сережиком решили заняться наукой, началось все с любимого эксперимента вулкан, который, я думаю, многие любят) но сейчас не о нем)
Мы продолжаем участвовать в проекте Марии Юнак ИГРАЕМ В ФИЗИКУ и осень началась с игр с водой.
Вода — уникальное вещество! Мы с вами гораздо больше, чем на половину состоим из воды, без воды не было бы жизни на Земле и т. д. Для начала мы поставили в окрашенную воду листики салата, что бы проследить, как пьют растения. Этот эксперимент остался на столе до утра.
Дальше я нарисовала простенькую картинку из чего состоит вода и Сереже очень понравился кислородик с ручками, который держит 2 маленьких водородика. Молекулу воды просто сделать из пластилина и зубочисток.
Сережа очень старался, но не удержался и каждому кислороду добавил антенну.
Молекулы готовы т мы перешли к агрегатным состояниям — жидкая, твердая и газообразная вода.
Во всех случаях молекула воды остается той же, но друг к другу они относятся уже по разному.
Структура льда четкая, молекулы крепко держатся за руки.
А вот паровички летят во все стороны! А еще пар умеет свистеть! Дада) нужен только чайник со свистком и ребенок удивлен и счастлив)
Ну а в жидком состоянии молекулы за руки тоже не держатся, но скучают друг по другу и просто тесняться поближе)
И еще мы провели увлекательный эксперимент с водой и свечкой! 2 таких любимых детьми вещи ОГОНЬ И ВОДА!
Здесь мы познакомились с теплоемкостью, любой горячий предмет, попадая в холодную воду, очень быстро охлаждается. Вода быстро забирает себе все тепло! Такое это уникальное вещество! Если капнуть парафин на твердую поверхность, например стола, то некоторое время парафин будет еще мягким и теплым, а в воде он моментально твердеет и остывает. И получаются очень красивые острова!
Вода быстро забирает себе все тепло! Такое это уникальное вещество! Если капнуть парафин на твердую поверхность, например стола, то некоторое время парафин будет еще мягким и теплым, а в воде он моментально твердеет и остывает. И получаются очень красивые острова!
Во всех экспериментах принимают участие Древние люди и животные, потому что это Сережины любимчики сейчас) и для них мы показали эксперимент с вулканом
Запечатлеть мне его не получилось, так как я занималась уксусом, и нужен глаз да глаз!
Рецепт прост- сам вулкан — это обрезанная банка, облепленная пластилином, она крепится к одноразовой тарелке тоже пластилином. Ставим его на поднос с бортами, далее лава — уксус, сода, красная краска, капля фэйри. Все засыпаем в жерло и льем уксус! Супер быстрый, секундный, но очень впечатляющий эксперимент! Запаситесь содой и уксусом — ребенок потребует еще и еще! Можно вместо уксуса взять лимонную кислоту, но эффект будет слабее.
Выливаем лаву аккуратненько, ребенку плескаться не даем. Я это делаю в резиновых перчатках, показывая опасность) хорошо бы еще очками обзавестись для опытов.
Я это делаю в резиновых перчатках, показывая опасность) хорошо бы еще очками обзавестись для опытов.
Спасибо вам за внимание)
как сделать модель днк своими руками
Как сделать модель ДНК из обычных материалов
Ответы@Mail.Ru: из чего и как сделать модель днк?
Как сделать модель ДНК из обычных материалов
Видео обзор — Модель структуры ДНК — YouTube
Как сделать модель ДНК из обычных материалов
ДНК из пластилина ( Фото №1 )
СМИ: ученые обнаружили ген, защищающий от инсульта, инфаркта и …
Как сделать модель ДНК из обычных материалов
Как сделать модель ДНК из обычных материалов
Как сделать модель ДНК из обычных материалов
Как сделать модель ДНК из обычных материалов
Как сделать модель ДНК из обычных материалов
Как сделать модель ДНК
Ген\u2013оракул и его толкователи | Публикации | Вокруг Света
Как сделать модель ДНК
Как сделать модель ДНК
Как сделать модель ДНК
molbiol. ru -\u003e Как проверить структуру белка?
ru -\u003e Как проверить структуру белка?
Строение молекулы ДНК — YouTube
Ген\u2013оракул и его толкователи | Публикации | Вокруг Света
Молекулы из пластилина. Пошаговый урок лепки.
3D-печать моделей молекул белка / Хабр
ДНК-оригами: путь от гравюры до нанороботов длиной в 30 лет
Молекулы из пластилина. Пошаговый урок лепки.
Молекулы из пластилина. Пошаговый урок лепки.
ДНК-оригами: путь от гравюры до нанороботов длиной в 30 лет
Модель Молекулы Метана Из Пластилина Фото
День днк фото \u2014 Поиск по картинкам \u2014 [RED]
ДНК-оригами: путь от гравюры до нанороботов длиной в 30 лет
Игорь Юдкевич — ДНК: Структура выяснена, а головоломка до сих пор не . ..
..
Конструктор жизни | Наука | ИноСМИ — Все, что достойно перевода
Вязаные… ДНК, молекула, нейрон и сердце
ДНК-оригами: путь от гравюры до нанороботов длиной в 30 лет
ДНК-оригами: путь от гравюры до нанороботов длиной в 30 лет
6.2. Модель молекулы ДНК: модель двойной спирали ДНК Утсона и Крика …
Опыты по химии. Шаростержневые модели молекул — YouTube
18 проектов Илона Маска: куда идут инвестиции технопредпринимателя …
Модель Молекулы Метана Из Пластилина Фото
В Бресте отец благодаря ДНК-экспертизе через 35 лет нашел дочь
Джеймс Уотсон, Эндрю Берри, Кевин Дэвис: «ДНК. История генетической …
Воры генов: почему британские ученые изучают мнения россиян о ДНК . ..
..
454-секвенирование (высокопроизводительное пиросеквенирование ДНК)
Молекулы из пластилина. Пошаговый урок лепки.
Элементарно, Уотсон! | Все блоги | Блоги | Каспаров.Ru
Биохакер учит людей самостоятельно менять свою ДНК
Генетический анализ ДНК. Генетическая диагностика
Своими руками: модель МТЛБ из металла в масштабе 1:18 (19 фото)
В одном экземпляре: возможности персонифицированной медицины …
Игорь Юдкевич — ДНК: Структура выяснена, а головоломка до сих пор не …
Как открывали структуру ДНК — Life Science links
Модель клетки из пластилина | МОРЕ творческих идей для детей
Джеймс Уотсон, Эндрю Берри, Кевин Дэвис: «ДНК. История генетической …
История генетической …
Структура Холлидея \u2014 Википедия
Кто открыл ДНК? Значение открытия ДНК. Фридрих Мишер
ДНК из полимерной глины
ДНК». Глава из книги \u2022 Д. Уотсон \u2022 Книжный клуб на «Элементах …
С матери-одиночки медики вымогают 26 тысяч за тест на отцовство
Игорь Юдкевич — ДНК: Структура выяснена, а головоломка до сих пор не …
Практический курс ДНК-генеалогии (18 видео-лекций) | Переформат.ру
Игорь Юдкевич — ДНК: Структура выяснена, а головоломка до сих пор не …
ДНК». Глава из книги \u2022 Д. Уотсон \u2022 Книжный клуб на «Элементах …
Изваяние невидимого
Модель клетки из пластилина | МОРЕ творческих идей для детей
Вирусная природа днк
На рынок выходит дешифратор ДНК в виде USB-флэшки
Разработаны в 100 000 раз более быстрые ДНК-нанороботы
Модель клетки из пластилина | МОРЕ творческих идей для детей
Анализ ДНК помогает искать преступников и предупреждать рак | Наука . ..
..
Миф о древних ДНК-генеалогических линиях африканцев (часть 1 …
ДНК: На что похожа главная молекула нашего тела? — Блог издательства …
Игорь Юдкевич — ДНК: Структура выяснена, а головоломка до сих пор не …
Звезда «Игры престолов» из России раскрыл, как строить карьеру в Голливуде
https://static.news.ru/photo/1039843c-bf76-11eb-bae7-96000091f725_660.jpg Юрий Колокольников в сериале «Игра Престолов» Фото: Game of Thrones/facebook.comРоссийский актёр Юрий Колокольников в беседе с порталом PeopleTalk раскрыл, как его коллегам из РФ построить карьеру за рубежом. Звезда четвёртого сезона фэнтези-саги «Игра престолов» уверен, что фраза «покорить Голливуд» уже устарела. По его словам, заокеанская кинофабрика «давно уже здесь — у тебя в компьютере, на стриминговых платформах».
Собеседник издания уверен, что для успешной работы за рубежом нужен хороший английский язык, а также необходимо разбираться в драматургии
Большое упущение наших актёрских школ, что в них артистов не учат разбирать материал, читать и понимать сценарий. Что такое структура сценария, какие законы в драматургии? Это важно, потому что когда ты выстраиваешь роль, ты составляешь для себя некую дорожную карту, и необходимо понимать нюансы, — считает Колокольников.
Он отметил, что в первую очередь артисты — это исполнители, гибкие, словно пластилин, они воплощают в жизнь написанное на бумаге. Но если выступать соавтором ролей, то характеры получатся намного точнее. Говоря о себе как об актёре, Колокольников ответил кратко: «Одним словом — гений». И засмеялся.
Колокольников известен ролями в «Доводе» Кристофера Нолана, «Призрачной шестёрке» Майкла Бэя, «Телохранителе киллера» Патрика Хьюза. В четвёртом сезоне «Игры престолов» он сыграл предводителя теннов Стира.
Ранее сообщалось, что американские актёры Дженнифер Энистон и Дэвид Швиммер, игравшие влюблённых Рейчел и Росса в сериале «Друзья», признались в настоящих чувствах друг к другу во время съёмок специального выпуска «Друзья: Воссоединение», вышедшего на сервисе HBO Max. Ведущему шоу Джеймсу Кордену удалось разговорить звёзд, и они раскрыли подробности отношений.
Добавить наши новости в избранные источники
Опровергнута самая популярная теория строения воды
Учёные СФУ совместно с коллегами из Королевского института технологий Швеции опровергли самую популярную ныне кластерную теорию строения воды. В ходе работы исследователи предложили новую теорию, согласующуюся с результатами их эксперимента. Работа опубликована в журнале Nature Communications. Исследования поддержаны грантом Российского научного фонда.
Вода — одно из самых распространённых, но в то же время необычных веществ на Земле. Она обладает рядом нетипичных свойств, объясняемых её особой структурой, например, высокой теплоёмкостью и низкой электропроводностью. Общепринято, что вода состоит из молекул Н2О, объединённых в группы так называемыми водородными связями. Их наличие обусловлено притяжением между положительно заряженными атомами водорода и отрицательно заряженными атомами кислорода. Свободные, не входящие в кластеры (группы молекул, связанных водородными связями) молекулы присутствуют лишь в небольшом количестве. Многие учёные считают, что вода — постоянно изменяющаяся смесь кластеров лёгкого и тяжёлого типов. В первом молекулы связаны друг с другом (как во льду), а во втором связи нарушены, благодаря чему такие системы более плотные. Наличие этих фаз можно обнаружить при помощи резонансного неупругого рассеяния рентгеновских фотонов водой. При этом виден переход, в котором электрон с занятой молекулярной орбитали заполняет дырку, на месте которой был выбитый ранее фотоном электрон. Эксперимент с жидкой водой показывает расщепление резонанса на два пика. В научной литературе получившийся дублет приписывается кластерам лёгкого и тяжёлого типов.
Общепринято, что вода состоит из молекул Н2О, объединённых в группы так называемыми водородными связями. Их наличие обусловлено притяжением между положительно заряженными атомами водорода и отрицательно заряженными атомами кислорода. Свободные, не входящие в кластеры (группы молекул, связанных водородными связями) молекулы присутствуют лишь в небольшом количестве. Многие учёные считают, что вода — постоянно изменяющаяся смесь кластеров лёгкого и тяжёлого типов. В первом молекулы связаны друг с другом (как во льду), а во втором связи нарушены, благодаря чему такие системы более плотные. Наличие этих фаз можно обнаружить при помощи резонансного неупругого рассеяния рентгеновских фотонов водой. При этом виден переход, в котором электрон с занятой молекулярной орбитали заполняет дырку, на месте которой был выбитый ранее фотоном электрон. Эксперимент с жидкой водой показывает расщепление резонанса на два пика. В научной литературе получившийся дублет приписывается кластерам лёгкого и тяжёлого типов.
Чтобы пролить свет на эту фундаментальную проблему, авторы работы провели эксперимент с парами воды, где нет водородных связей. В ходе исследования они измерили спектр резонансного неупругого рассеяния изолированной молекулы. Эксперименты привели к неожиданному результату и показали, что точно такое же расщепление резонанса на два пика присутствует в рентгеновских спектрах рассеяний молекул воды в газовой фазе. Более того, выполненные теоретические расчёты однозначно объясняют расщепление на спектре сверхбыстрым распадом (диссоциацией) молекулы воды на ионы Н+ и ОН-. Таким образом, исследование свидетельствует о динамической природе расщепления резонанса и опровергает структурный механизм, тем самым демонстрируя, что структура воды однородна.
Второй не менее важный результат этой работы — получение детальной структурной информации о том, как влияют водородные связи на силу OH-связи. Колебательная инфракрасная (ИК) спектроскопия — общепринятый инструмент для исследования водородных связей в жидкостях. Но в них ИК-спектроскопия показывает лишь наиболее интенсивный переход в состояние с минимальной энергией колебаний, которое «слабо чувствует» межмолекулярное взаимодействие. Спектроскопия резонансного неупругого рассеяния воды качественно отличается от ИК-спектроскопии тем, что, получив энергию от рентгеновского фотона, электрон кислорода переходит с самой глубокой орбитали на первую незанятую. В результате молекула воды быстро диссоциирует. В процессе возбуждённый электрон переходит обратно на самый глубокий уровень, испуская рентгеновский фотон. Частота колебаний испущенного фотона отличается от возбуждающего фотона, так как при этом переходе электрон попадает на уровни с большей энергией. Таким образом, в отличие от ИК-спектра, спектр резонансного неупругого рассеяния состоит из протяжённого набора колебательных пиков. Чем выше колебательное состояние, тем дальше атомы водорода удаляются от кислорода в процессе колебаний связи между О и Н и тем сильнее это колебание чувствует взаимодействие с ближайшей молекулой воды, а именно водородную связь. Резонансное неупругое рассеяние даёт уникальную возможность исследовать водородные связи, в частности определить на основании спектра, как влияют соседние молекулы через водородную связь на потенциал взаимодействия OH-связи.
Но в них ИК-спектроскопия показывает лишь наиболее интенсивный переход в состояние с минимальной энергией колебаний, которое «слабо чувствует» межмолекулярное взаимодействие. Спектроскопия резонансного неупругого рассеяния воды качественно отличается от ИК-спектроскопии тем, что, получив энергию от рентгеновского фотона, электрон кислорода переходит с самой глубокой орбитали на первую незанятую. В результате молекула воды быстро диссоциирует. В процессе возбуждённый электрон переходит обратно на самый глубокий уровень, испуская рентгеновский фотон. Частота колебаний испущенного фотона отличается от возбуждающего фотона, так как при этом переходе электрон попадает на уровни с большей энергией. Таким образом, в отличие от ИК-спектра, спектр резонансного неупругого рассеяния состоит из протяжённого набора колебательных пиков. Чем выше колебательное состояние, тем дальше атомы водорода удаляются от кислорода в процессе колебаний связи между О и Н и тем сильнее это колебание чувствует взаимодействие с ближайшей молекулой воды, а именно водородную связь. Резонансное неупругое рассеяние даёт уникальную возможность исследовать водородные связи, в частности определить на основании спектра, как влияют соседние молекулы через водородную связь на потенциал взаимодействия OH-связи.
«Важно отметить, что, в отличие от изолированной молекулы воды с одной энергией взаимодействия О и Н, в жидкости имеется набор (распределение) таких энергий в силу многообразия ближайшего окружения молекулы воды. Таким образом, второй результат работы — измерение распределения OH-потенциалов в сети постоянно изменяющихся водородных связей. На следующем этапе исследований необходимо выяснить, возможно ли из спектров резонансного неупругого рассеяния воды определить такой важный структурный параметр, как среднее число связей молекулы. Он определяет энергию взаимодействия последней с её окружением, а значит, и такие свойства, как скорость звука в воде и её теплоёмкость»,— дополняет Фарис Гельмуханов, доктор физико-математических наук, профессор Королевского технологического института (Стокгольм, Швеция), старший научный сотрудник Сибирского федерального университета.
В работе также приняли участие учёные из Университета Потсдама (Германия), Университета Цюриха (Швейцария) и Университета Турку (Финляндия).
Рисунки
- A) Молекула воды, поглотив фотон, возбуждается из основного состояния (0) в высоковозбуждённое диссоциативное состояние (с), где атом водорода быстро покидает точку равновесия. В процессе диссоциации возбуждённая молекула возвращается в основное (0) или конечное состояние (f) испуская другой фотон и формируя спектр вблизи 535 эВ и 526 эВ, соответственно.
- Б) рентгеновский спектр поглощения воды.
- B) Спектры испускания c→f и c→0 вблизи 526 эВ и 535 эВ, соответственно. Эмиссионный спектр c→f вблизи 525 эВ показывает динамическое формирование (в процессе диссоциации) дублета с расщеплением Δ (см. панель A). При возвращении молекулы в основное состояние c→0 в процессе диссоциации заселяются высокие колебательные уровни, что формирует протяжённую колебательную прогрессию в районе 535 эВ.
- Г) В работе решена обратная задача восстановления из колебательной прогрессии распределения OH-потенциалов воды в жидкой фазе.
Пресс-служба РНФ, пресс-служба СФУ,
причин создавать собственные молекулярные модели | Идеи
Многое из того, что мы знаем о химии, невозможно увидеть. Вместо этого ученые разработали модели для описания ключевых концепций на основе имеющихся данных и математических принципов. Модели можно рассматривать как инструменты мышления, помогающие формировать объяснения. Они также являются полезными упрощениями для облегчения понимания.
Физическое моделирование в классе химии — хороший способ помочь студентам визуализировать такие понятия, как молекулярная геометрия, структура и связи, атомная структура и теория столкновений.Хотя теория «стилей обучения» в преподавании и обучении была широко дискредитирована, кинестетические подходы — учебная деятельность, предполагающая выполнение определенных действий — действительно добавляют разнообразия урокам для учителей и учеников. Физические модели также могут стимулировать обсуждение между учениками или способствовать дискуссии между учеником и учителем.
Наборы молекулярных моделей часто используются для физического моделирования в классе химии. Атомы и соединения в наборах молекулярных моделей были специально разработаны для воспроизведения наблюдаемых углов и валентностей атомов в ковалентных молекулах.Однако комплекты могут быть дорогими и ограничивать моделирование школьной средой. Неформальное моделирование с использованием доступных материалов — доступная альтернатива. Одно исследование, посвященное неформальному моделированию молекулярной геометрии, показало, что наборы для самостоятельной сборки с использованием очистителей труб оказались «более значимыми для лучших учеников и более приятными для всех».
Наборы молекулярных моделей часто используются для физического моделирования в классе химии.Атомы и соединения в наборах молекулярных моделей были специально разработаны для воспроизведения наблюдаемых углов и валентностей атомов в ковалентных молекулах. Однако комплекты могут быть дорогими и ограничивать моделирование школьной средой. Неформальное моделирование с использованием доступных материалов — доступная альтернатива. Одно исследование, посвященное неформальному моделированию молекулярной геометрии, показало, что наборы для самостоятельной сборки с использованием очистителей труб оказались «более значимыми для лучших учеников и более приятными для всех». 1
Выбор материалов для моделирования
Вы можете найти примеры концепций химии, смоделированные с использованием всех мыслимых материалов в академической литературе и в других местах. Сферы, представляющие атомы, можно смоделировать из таких материалов, как полистирольные шары, пластилин или липкую ленту. Атомные соединения можно смоделировать с помощью очистителей для труб, ватных палочек или зубочисток. В совокупности они похожи на модели, сделанные с помощью наборов молекулярных моделей. Студентам необходимо решить, сколько связей установить и где их разместить, что создает трудности для более успешных.Строительные леса могут поддержать студентов, нуждающихся в дополнительной помощи.
В вашем классе
Загрузите рабочий лист по созданию модели связывания в аммиаке в формате MS Powerpoint или pdf.
Склеивающие модели могут быть изготовлены из аналогичных материалов. Формы картонных головоломок или перфокарты могут представлять собой ионы. Очистители труб в виде валентных оболочек и бусинок в качестве внешних электронов могут проиллюстрировать модель ковалентной связи Льюиса.Нить, картонные круги или проволока образуют электронные оболочки для модельных атомов, а липкие точки, глазки, ювелирные бусинки и даже сладости могут показывать электроны.
Склеивающие модели могут быть изготовлены из аналогичных материалов. Формы картонных головоломок или перфокарты могут представлять собой ионы. Очистители труб в виде валентных оболочек и бусинок в качестве внешних электронов могут проиллюстрировать модель ковалентной связи Льюиса. 2 Нитка, картонные кружки или проволока образуют электронные оболочки для модельных атомов, а липкие точки, глазки, ювелирные бусинки и даже сладости могут показывать электроны.
Получение максимальной отдачи от физических моделей
Учителям сложно использовать модели, потому что могут возникнуть неправильные представления. Например, распространено заблуждение, что научная модель — это точная копия реальной вещи, точно так же, как литая под давлением игрушечная машинка является моделью транспортного средства стандартного размера. Немногие студенты понимают, почему ученые используют несколько моделей для объяснения концепций. Кроме того, слово «модель» имеет несколько значений в зависимости от контекста. Когда мы используем слово «образец» в обучении, то, что приходит в голову нашим ученикам, скорее всего, будет отличаться от того, что находится в нашей голове.
Учителям сложно использовать модели, потому что могут возникнуть неправильные представления. Например, распространено заблуждение, что научная модель — это точная копия реальной вещи, точно так же, как литая под давлением игрушечная машинка является моделью транспортного средства стандартного размера. Немногие студенты понимают, почему ученые используют несколько моделей для объяснения концепций. 3 Кроме того, слово «модель» имеет несколько значений в зависимости от контекста. Когда мы используем слово «образец» в обучении, то, что приходит в голову нашим ученикам, скорее всего, будет отличаться от того, что находится в нашей голове.
Как и в любой другой классной деятельности, вы должны оценить учебные цели, сопровождающие моделирование, и спланировать другие аспекты урока, чтобы учащиеся добивались успехов. Уроки моделирования произвольной формы редко бывают успешными. Поэкспериментируйте с материалами перед уроками, чтобы предвидеть, где могут возникнуть неправильные представления или даже неправильное поведение. Подумайте, какие вопросы будут проверять понимание учащимися и как вопросы и размышления будут работать в больших классах. Например, пачки карточек с вопросами между парами учащихся служат подсказками для обсуждения.Они позволяют учителю продолжить в конце урока с помощью прямых вопросов, как только ученики получат возможность подумать.
Помимо урока, неформальные модели служат хорошим дисплеем в классе, обеспечивая надолго запоминание. Поскольку они недорогие, студенты могут забрать их домой или использовать материалы из дома, чтобы делать модели и критиковать их.
Нам бы очень хотелось увидеть, как вы занимаетесь неформальным моделированием во время занятий. Напишите нам в Твиттере @RSC_EiC.
Лучшие советы для неформального моделирования
1.Обдумайте логистику распределения материалов и уборки.
2. Предвидите, какие проблемы могут возникнуть в результате использования выбранных вами материалов, например, проблемы с гигиеной для сладостей в лабораториях и проблемы с безопасностью для чистящих средств для острых труб.
3. Запланируйте опрос для более глубокого анализа теории или проверки полезности модели.
Кристи Тернер — научный сотрудник Манчестерского университета / школы Болтона
Дополнительная литература
Королевское химическое общество Разработка и использование моделей Курс CPD помогает справиться с трудностями, связанными с использованием моделей.
Список литературы
1. T. Kenney, J. Chem. Educ. , 1992, 69 , 67, (DOI: 10.1021 / ed069p67)
2. К. Л. Тернер, J. Chem. Educ. , 2016, 93 , 1073, (DOI: 10.1021 / acs.jchemed.5b00981)
3. Д. Ф. Треагуст и А. Г. Харрисон , Int. J. Sci. Образов., 2000, 22 , 1011, (DOI: 10.1080 / 095006
6884)Руководство для начинающих по построению и визуализации молекул в программном обеспечении молекулярной графики с открытым исходным кодом
BMC Res Notes.2021; 14: 66.
иSiripreeya Phankingthongkum
Научный отдел, Международный колледж Университета Махидол, Университет Махидол, Салая, Пхуттамонтон, Накхонпатхом, 73170 Таиланд
Международный университет Тавитхама Лимпанупарб, Международный научный колледж Махидола
, Университет Махидол, Салая, Пхуттамонтон, Накхон Патом, 73170 Таиланд
Отдел науки, Международный колледж Университета Махидол, Университет Махидол, Салая, Пхуттамонтон, Накхон Патом, 73170 Таиланд
Автор, отвечающий за переписку.Поступило 05.11.2020 г .; Принято 22 января 2021 г.
Открытый доступ Эта статья находится под лицензией Creative Commons Attribution 4.0 International License, которая разрешает использование, совместное использование, адаптацию, распространение и воспроизведение на любом носителе или любом формате при условии, что вы надлежащим образом укажете оригинал Автор (ы) и источник предоставляют ссылку на лицензию Creative Commons и указывают, были ли внесены изменения. Изображения или другие сторонние материалы в этой статье включены в лицензию Creative Commons для статьи, если иное не указано в кредитной линии для материала.Если материал не включен в лицензию Creative Commons для статьи и ваше предполагаемое использование не разрешено законом или превышает разрешенное использование, вам необходимо получить разрешение непосредственно от правообладателя. Чтобы просмотреть копию этой лицензии, посетите http://creativecommons.org/licenses/by/4.0/. Отказ Creative Commons Public Domain Dedication (http://creativecommons.org/publicdomain/zero/1.0/) распространяется на данные, представленные в этой статье, если иное не указано в кредитной линии для данных.- Дополнительные материалы
Дополнительный файл 1. Рабочий лист и файлы для студентов.
GUID: 32F53857-8DC4-48ED-9A60-93704EBAF0D9
Дополнительный файл 2. Критерии оценки и полные решения, включая дополнительные упражнения.
GUID: 4863F12D-9FDF-4B40-856A-7CDEDB2A5DD1
Дополнительный файл 3. Вопросы исследования и подробные результаты.
GUID: 77BC443F-D0E8-4A13-A2BF-EEAA17F5BE55
- Заявление о доступности данных
Наборы данных, подтверждающие выводы этой статьи, доступны в репозитории данных Mendeley по адресу https: // doi.org / 10.17632 / hfynpvtrz3: Руководство, содержащее скриншоты с пошаговыми инструкциями по выполнению поставленных задач и видео с примерами процесса.
Реферат
Цель
Представлено приложение для молекулярной графики в качестве простой и бесплатной альтернативы наборам молекулярных моделей для изучающих химию начального уровня.
Результаты
На основе Avogadro или IQmol мы предложили студентам четыре набора задач, построение базовой молекулярной геометрии, визуализацию орбиталей и плотностей, предсказание полярности молекул и сопоставление трехмерных структур со структурами линий связи.Эти темы обычно охватываются общей химией для студентов первого курса бакалавриата. Для всех задач обеих программ предусмотрены подробные пошаговые процедуры, чтобы преподаватели и студенты могли использовать одну из двух программ в своем обучении и обучении в качестве альтернативы наборам молекулярных моделей.
Ключевые слова: Химическое образование, Молекулярная модель, Общая химия, Программное обеспечение для молекулярной графики
Введение
Использование молекулярной модели рекомендовано в качестве части учебной программы для улучшения пространственного мышления студентов-химиков [1].Наборы физических молекулярных моделей обычно используются в химической лаборатории начального уровня [2]. Другие аналогичные учебные пособия [3–45] сильно различаются по стоимости, простоте использования, необходимому количеству времени и пригодности для изучения соответствующих тем по химии. Мы рассмотрели и попробовали некоторые из них в нашем классе и пришли к некоторым наблюдениям. В таблице представлен краткий обзор литературы и наши наблюдения по некоторым физическим молекулярным моделям.
Таблица 1
Краткий обзор средств обучения молекулярным моделям и наши наблюдения над некоторыми физическими молекулярными моделями
| Средства обучения молекулярным моделям | Наши наблюдения |
|---|---|
Физические молекулярные модели o Мячи для пинг-понга [3], резиновые шары [4], крышки от бутылок [5, 6], маркеры для белых досок [7] или другие материалы [8–14] (Использование имеющихся материалов) o Пластилин [15], глина или тесто [16], (ручное строительство из податливых материалов) o Лазерная / проволочная резка [17], 3D-печать [18–21], 3D-лазерная гравировка [22], силикон, залитый магнитом [23] модели с помощью передовых методов) Компьютерное программное обеспечение или веб-приложения o Специализированные онлайн-сервисы, такие как молекулярные кликеры на основе 3Dmol.js [24], Android-приложение для химического распознавания символов и трехмерной визуализации [25], моделирования элементарных ячеек [26] и моделирования формы молекул [27] o Платоновые твердые тела на языке POV-Ray [28] или орбитальные дисплеи в системе Mathematica [29] ] o Программное обеспечение для молекулярной графики o Собственное коммерческое программное обеспечение, например GaussView [30], Chem3D [31] o Программное обеспечение с открытым исходным кодом, например Avogadro [32, 33], Chimera [34], Gabedit [35], IQmol [36], PyMOL [37] и QuteMol [33] o Онлайн-сервис для молекулярной графики, такой как WebMO [38] и CheMagic [39]) 3D / дополненная реальность (Расширенные методы визуализации обычно требуют для работы как специального оборудования, так и программного обеспечения.) o 3D-видеоочки [40, 41] o Приложение на мобильных устройствах [42–44] o Голографическая проекция [45] | ● Коммерческие наборы молекулярных моделей могут быть дорогостоящими единовременными вложениями. Поскольку в набор входит множество элементов, представляющих различные типы атомов / связей, пользователи молекулярных моделей обычно тратят значительное количество времени на инвентаризацию. Время может быть сокращено, если для этого процесса подсчета используются аналитические весы. Во многих случаях учащиеся также тратят много времени или сталкиваются с трудностями при разборке моделей до их первоначальных частей.Эта разборка обычно необходима перед построением следующих молекул, поскольку стандартный набор молекулярных моделей из 165 частей содержит только 14 атомов углерода. ● Другие физические модели (например, мячи для настольного тенниса и пластилин) могут иметь свои плюсы и минусы. Например, пластилин пластичен и из него можно формировать шариковые и палочные модели, а также модели, заполняющие пространство. Мы попросили студентов взвесить пластилин, чтобы они вручную строили модели, пропорциональные реальным молекулам. Студенты четко наблюдали относительный размер водорода по сравнению с галогеном в галогенидах водорода и правильно предсказали тенденцию кислотности.Однако использование пластилина может быть утомительным, грязным и отвлекающим для некоторых учеников. |
Программное обеспечение для молекулярной графики доступно на рынке уже много десятилетий. До недавнего времени эти программы предназначались для опытных пользователей моделирования квантовой и молекулярной механики и лицензировались по высокой цене. С лицензированием с открытым исходным кодом стоимость и доступность программного обеспечения больше не являются проблемой.
Большинство программ молекулярной графики позволяют пользователям конструировать, редактировать и визуализировать молекулы в 3D и, следовательно, являются жизнеспособной альтернативой обычным учебным материалам.Поэтому проблема здесь в том, как использовать эти динамические и интерактивные программы визуализации в качестве строительных инструментов для обучения студентов [46]. В ряде статей описано использование этого программного обеспечения для обучения студентов старших курсов [24, 25, 31, 33, 34, 47, 48]. Однако учебные упражнения по химии начального уровня ограничены, поскольку эти программы считаются специализированными и используются в основном для исследований.
В этой статье описывается наш опыт использования двух программ, Avogadro и IQmol, для урока в лабораторных занятиях по химии вводного уровня.Урок был разработан таким образом, чтобы максимально соответствовать содержанию, которое преподается по общей химии. Расширенные функции, традиционно связанные с использованием этих программ, намеренно не учитываются. Насколько нам известно, наша работа является первой статьей, в которой подробно описывается использование программного обеспечения для молекулярной графики в образовательных целях для этого уровня аудитории.
Лабораторный курс — первая лаборатория химии для студентов естественных наук. Урок можно пройти независимо от лекционного класса. Цели этого четырехчасового сеанса с программным обеспечением:
использовать виртуальный инструмент таким же образом, как используются физические молекулярные модели (задачи 1 и 4 ниже)
для использования некоторых дополнительных функций визуализации программное обеспечение, связанное с обсуждаемым в курсе общей химии, без выполнения квантово-химического расчета (задачи 2 и 3 ниже).
Инструкции составлены таким образом, чтобы учащиеся могли легко выполнять их даже без предварительных знаний по химии, а учащиеся также могли оценить качество изображений учебного качества. Из-за четкого разделения лаборатории и лекции в учебной программе мы не намерены преподавать базовые концепции, а только предоставлять инструменты и практики для поддержки их обучения.
Описание программного обеспечения и функций
Avogadro [32] и IQmol [36] — это кроссплатформенные программы с открытым исходным кодом для Mac и Windows, запущенные в 2016 и 2015 годах соответственно.Обе программы легки и просты в установке. Они предлагают ряд функций для выполнения и анализа вычислений. Каждая программа требует минимального дискового пространства (<50 МБ), и для большинства пользователей загрузка и установка может занять менее 5 минут. Программы также доступны для Linux, но установка может быть нетривиальной.
Как упоминалось ранее, в этой статье мы не собираемся знакомить новичков с выполнением каких-либо расчетов [47–49] или работой с какими-либо макромолекулами. Мы используем только следующие возможности программ.
o
Чтение различных типов файлов (геометрия xyz или z-матрицы, файл контрольных точек, выходные данные расчета частоты).
o
Создавайте и редактируйте молекулы с помощью графического пользовательского интерфейса и оптимизируйте структуры с помощью встроенных силовых полей молекулярной механики.
o
Визуализируйте молекулы в различных представлениях (шар и палка или заполнение пространства), а также отображая длину связи, угол связи и угол скручивания.
o
Некоторые из дополнительных функций, например отображение анимации, дипольного момента, спектров и поверхностей (орбиталей и плотностей).
Основной текст
Задачи учащегося и их выполнение
Упражнение с компьютерной молекулярной моделью внедрено в химической лаборатории первого года обучения в Университете Махидол с 2019 года. Рабочий лист студента в Дополнительном файле 1 был разработан и постоянно обновлялся. Студентам было предложено заполнить двухстраничный рабочий лист, состоящий из четырех наборов задач.Общее время на выполнение всех задач составляет примерно три-четыре часа. Наша деятельность проводится в компьютерной лаборатории в течение первой недели курса, поскольку студентам еще предстоит найти свой собственный лабораторный халат и защитные очки для химической лаборатории. В результате ознакомительный / демонстрационный сеанс безопасности [50] запланирован на вторую неделю, а реальный эксперимент начинается на третьей неделе. Это дает студентам и сотрудникам больше времени для завершения необходимых мероприятий и подготовки, связанных с лабораторным занятием.
Мы рекомендуем студентам использовать одну из двух программ, заранее установленных в нашей компьютерной лаборатории. Однако некоторые студенты хотят использовать свои собственные ноутбуки. Совершенно законно загружать / делиться и устанавливать эти программы с открытым исходным кодом на студенческие машины.
Учащиеся по-разному выполняют наши задания в зависимости от их компьютерной грамотности. Распределение их случайным образом на группы по два человека так же, как и другие лабораторные задания, частично помогает устранить разницу. Лучше всего продемонстрировать один пример из каждой задачи для четырех задач подряд.Мы убеждаемся, что все группы могут правильно выполнять примеры задач, прежде чем позволить им работать независимо. Студентам также предлагается продемонстрировать различные подходы к выполнению задач. (Скриншоты шагов для выполнения этих задач находятся в репозитории данных Mendeley.)
Дополнительные упражнения, выделенные желтым цветом в дополнительном файле 2, также рассматриваются ниже для этих задач. В то время как основные задачи требуют небольших предварительных знаний от лекционного класса или совсем не требуют их, эти дополнительные упражнения требуют некоторых базовых знаний.Обычно они более сложные и требуют много времени. Эти упражнения использовались в нашей предыдущей версии рабочего листа, но больше не используются в нашей текущей версии из-за нехватки времени и их сложности. Мы рекомендуем, при желании, включать только некоторые из этих упражнений для продвинутых учеников в соответствии с классом. Целью включения дополнительных упражнений в каждое задание было дать учащимся более прочную связь между заданиями и темами по химии.
Задание 1: Построение базовой молекулярной геометрии
Учащимся предлагается представить в виде шарика и палки 12 одноцентровых молекул на рабочем листе, как показано на рис.. Молекулы являются типичными примерами структур, охватываемых теорией VSEPR. В этом задании учащиеся выбирают xyz-файл молекулы-шаблона со стерическим числом от двух до шести и удаляют / заменяют атомы по мере необходимости. Такой подход построения по шаблону позволяет программному обеспечению работать так же, как набор физических молекулярных моделей. Все длины связей и углы не меняются, когда учащиеся строят новую молекулу путем удаления или замены атомов из шаблона.
Образец заданий 1 и 2, в которых студенты строят молекулы из различных шаблонов и визуализируют орбитали атомов водорода в IQmol.
Дополнительное упражнение состоит из различных задач.Найдите начало каждого валентного угла в таблице, включая угол ~ 109,5 ° для тетраэдрической структуры. Найдите структуру дополнительной молекулы для теории VSEPR. Визуализируйте молекулу в модели, заполняющей пространство. Примените силовое поле к молекулам и используйте правило Бента, чтобы объяснить отклонение от ожидаемого угла связи ~ 109,5 ° в аммиаке и воде и небольшое различие в длине связи C-H в метане и галометанах [51].
Задача 2: Визуализация орбиталей и плотностей
Два файла контрольных точек заранее подготовлены для учащихся для визуализации поверхностей в программном обеспечении.Исследуются молекулярные орбитали (МО), такие как самая высокая занятая молекулярная орбиталь (ВЗМО) и самая низкая незанятая молекулярная орбиталь (НСМО). Учащиеся используют первый файл для визуализации атомных орбиталей (1s, 2s, 3s, 2p, 3p и 3d) атома водорода. Второй файл формальдегида используется для построения HOMO, LUMO и карты полной электронной плотности молекулы. Студенты оценивают формы и относительные размеры атомов и молекул на карте плотности.
Необязательным упражнением является наблюдение за влиянием различных значений ISO на результаты и изучение других функций рендеринга, таких как рендеринг сетки и обрезка.
Задание 3: Предсказание полярности молекул
Учащиеся строят молекулу, создают цветную карту электростатического потенциала, показывают частичные заряды на атомах и показывают стрелку дипольного момента на каждой молекуле. Это помогает студентам понять концепции электроотрицательности, резонансной структуры, дипольного момента связи и полярности молекул.
Необязательное упражнение — изучить колебательную спектроскопию из заданного выходного файла квантово-химических расчетов. Учащиеся могут наблюдать колебательный режим молекулы на разных частотах в анимации, а также наблюдать за ее инфракрасным / рамановским спектром.Задача не только позволяет студентам пользоваться интерактивной функцией программного обеспечения, но и связывает понятие дипольного момента с правилом выбора в колебательной спектроскопии.
Задача 4: Сопоставление трехмерных структур со структурами линий связи
Студентам предоставляется набор файлов геометрии, которые они могут открыть с помощью программы. Студенты сопоставляют каждую трехмерную визуализацию в программе с двухмерной структурой линий связи, например. Проекция Фишера, проекция Ньюмана, конформация кресла. Учащиеся могут записать имена файлов под этими структурами в таблицах рабочего листа.
Дополнительное упражнение включает идентификацию всех энантиомеров, диастереомеров и ротамеров вместе с ранжированием их стабильности; изменение структуры кресла замещенного циклогексана на другую структуру кресла; и построение более сложных молекул, таких как парацетамол и аспирин. Кроме того, однобуквенные имена файлов в основной задаче сопоставления, приведенной выше, могут быть заменены систематическими или общими именами. В процессе студенты будут ознакомлены с названиями этих химических структур.
Результаты и обсуждение
Мы разработали новое лабораторное упражнение для начинающих студентов-химиков по изучению молекулярного моделирования. Использование компьютерных программ для урока молекулярной модели помогает преодолеть традиционные трудности и предлагает большую гибкость в преподавании и обучении. Значительная часть наших задач требует, чтобы студенты документировали свою работу, помещая изображения в рабочий лист. Эти изображения более или менее похожи на рисунки в большинстве учебников по общей химии и помогают студентам подготовиться к изучению химических понятий или закрепить их на лекциях.У нас есть ограниченные доказательства того, что учащиеся позже используют приобретенные здесь навыки для создания высококачественного изображения для последующих задач в классе [52, 53].
Хотя эти задачи предназначены для очного выполнения, в период вспышки COVID-19 задачи были выполнены удаленно в мае 2020 года и январе 2021 года с минимальными изменениями. Инструктор (TL) и ассистент преподавателя (SP) проводили обучение студентов в режиме реального времени. Студенты по-прежнему работали парами и отправляли по одному листу на пару во время урока, как мы обычно делаем в классе на территории кампуса.Некоторые из наших студентов сообщили о технических проблемах с одной из двух программ дома. Затем мы предложили им попробовать другую программу для решения проблемы.
Предварительные и последующие тесты использовались в классе на территории кампуса в сентябре 2020 года для оценки успеваемости студентов во время лабораторных упражнений. Средний балл ученика в классе из 31 ученика увеличился с 63% до 74% после выполнения заданий. Вопросы плюс / минус / дельта были частью заключительного теста. Подробные комментарии можно найти в Дополнительном файле 3.Вкратце, студенты используют следующие слова для описания своего положительного опыта, например ( n = 8), см. ( n = 9), визуализировать / визуально ( n = 5), интересно ( n = 2). ) и понять ( n = 2). Область, требующая улучшения, включает в себя управление временем в классе и темпами обучения.
В заключение, перепрофилирование двух свободно доступных программ молекулярной графики, Avogadro и IQmol, из специализированных применений в образовательные для начинающих, как описано в этой статье, является жизнеспособной альтернативой традиционным наборам молекулярных моделей.Эти простые упражнения можно использовать в других классах, других доступных программах или онлайн-сервисах [38, 39] с минимальными усилиями. Более того, эти мероприятия можно легко проводить в режиме онлайн, чтобы обеспечить соблюдение требований физического дистанцирования во время пандемии.
Ограничения
Некоторые концепции, такие как порядок облигаций и резонанс, могут быть плохо представлены в программах. Другие концепции, такие как формальный заряд атома, общий заряд структуры и несвязывающий электрон, могут быть недоступны для визуализации.
Количественное доказательство обучения в этой статье является предварительным (двустороннее значение p = 0,055 для класса в кампусе в сентябре 2020 г.), и на него может повлиять двойное прохождение параллельных тестов (в предварительном и пост-тесты).
Во избежание плагиата учащихся могут попросить создать видео с помощью встроенного средства записи экрана (XBox в Windows или Quicktime в Mac), чтобы показать процесс их работы.
Установка программ может быть ограничена политикой безопасности.«Невозможно проверить разработчика» — известная проблема, которую можно обойти.
Дополнительная информация
Благодарности
Мы ценим помощь технических специалистов (С. Фомсурин и В. Йимкосол), лаборантов (С. Датта, К. Кэвпичит, В. Лорпайбун и П. Таворнпарча) и студентов за их участие в классе. TL благодарит оргкомитет STT46 за приглашение представить эту работу на сессии «Ответственные химические науки для будущего устойчивого развития» конференции в Университете Рамкамхенг 6 октября 2020 года.
Аббревиатуры
| OCR | Оптическое распознавание символов | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| POV-Ray | The Persistence of Vision Ray Tracer | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| VSEPR | 9022 Теория оболочек 9022 9022 Отталкивание электронной пары SP и TL в равной степени внесли свой вклад в работу. TL задумал идею, получил финансирование и написал рукопись. SP провел исследование и анализ и написал рукопись под руководством TL.Оба автора прочитали и одобрили окончательный вариант рукописи. ФинансированиеЭто исследование было поддержано грантом на развитие научного сотрудника в середине карьеры (NRCT5-RSA63015-22), совместно финансируемым Национальным исследовательским советом Таиланда (NRCT) и Университетом Махидол. Финансирующие организации не играли никакой роли в дизайне исследования, сборе и анализе данных, принятии решения о публикации или подготовке рукописи. Доступность данных и материаловНаборы данных, подтверждающие выводы этой статьи, доступны в репозитории Mendeley Data, https: // doi.org / 10.17632 / hfynpvtrz3: Руководство, содержащее скриншоты с пошаговыми инструкциями по выполнению поставленных задач и видео с примерами процесса. Утверждение этических норм и согласие на участиеИсследование было одобрено IPSR-IRB Университета Махидол, сертификат одобрения № 2016 / 12-150 и 2020 / 05-241. Письменное информированное согласие было получено от всех участников. Несовершеннолетние (лица до 16 лет) в исследовании не участвовали. Согласие на публикациюНе применимо. Конкурирующие интересыАвторы заявляют, что у них нет конкурирующих интересов. СноскиПримечание издателя Springer Nature сохраняет нейтралитет в отношении юрисдикционных претензий на опубликованных картах и институциональной принадлежности. Дополнительная информацияОнлайн-версия содержит дополнительные материалы, доступные по адресу 10.1186 / s13104-021-05461-7. Ссылки1. Стулл А.Т., Хегарти М., Диксон Б., Стифф М.Репрезентативный перевод с конкретными моделями в органической химии. Cogn Instr. 2012. 30 (4): 404–434. DOI: 10.1080 / 07370008.2012.719956. [CrossRef] [Google Scholar] 2. Иствуд ML. Самые быстрые пальцы: игра о построении молекул для обучения органической химии. J Chem Educ. 2013. 90 (8): 1038–1041. DOI: 10.1021 / ed3004462. [CrossRef] [Google Scholar] 3. Элсворт К., Ли Б.Т., Тен А. Создание рентабельных кристаллических структур с мячами для настольного тенниса и лентой, которые позволяют студентам собирать и моделировать несколько элементарных ячеек.J Chem Educ. 2017; 94 (7): 827–828. DOI: 10.1021 / acs.jchemed.7b00305. [CrossRef] [Google Scholar] 4. Hoogenboom BE. Трехмерные модели атомных орбиталей. J Chem Educ. 1962. 39 (1): 40–41. DOI: 10.1021 / ed039p40. [CrossRef] [Google Scholar] 5. Сиодлак Д. Построение молекулярных моделей с помощью навинчивающихся крышек от бутылок. J Chem Educ. 2013; 90 (9): 1247–1249. DOI: 10.1021 / ed400126p. [CrossRef] [Google Scholar] 6. Сиодлак Д. Построение больших молекулярных моделей с помощью пластиковых навинчивающихся крышек для бутылок и прочных соединителей. J Chem Educ.2017; 94 (2): 256–259. DOI: 10.1021 / acs.jchemed.6b00576. [CrossRef] [Google Scholar] 7. Драгойлович В. Улучшение молекулярной модели размером с лекцию путем перепрофилирования использованных маркеров на белой доске. J Chem Educ. 2015; 92 (8): 1412–1414. DOI: 10.1021 / ed500964n. [CrossRef] [Google Scholar] 8. Тернер К.Л. Экономичное упражнение по физическому моделированию для развития у студентов понимания ковалентной связи. J Chem Educ. 2016; 93 (6): 1073–1080. DOI: 10.1021 / acs.jchemed.5b00981. [CrossRef] [Google Scholar] 9. Becker R. Конструкции мешалки для кофе.J Chem Educ. 1991; 68 (6): 459. DOI: 10.1021 / ed068p459. [CrossRef] [Google Scholar] 10. Kemp KC. Новая, простая и недорогая модель для обучения теории VSEPR. J Chem Educ. 1988; 65 (3): 222. DOI: 10.1021 / ed065p222. [CrossRef] [Google Scholar] 11. Хервас М, Сильверман LP. Магнитная иллюстрация теории VSEPR. J Chem Educ. 1991. 68 (10): 861–862. DOI: 10.1021 / ed068p861.2. [CrossRef] [Google Scholar] 12. Кондински А, Парак-Фогт Т.Н. Программируемые блокирующие диски: восходящая модульная сборка химически релевантных многогранных и сетчатых структурных моделей.J Chem Educ. 2019; 96 (3): 601–605. DOI: 10.1021 / acs.jchemed.8b00769. [CrossRef] [Google Scholar] 13. Кондински А., Мунс Дж., Чжан Й., Буссе Дж., Де Борггрейв В., Нис Е. и др. Моделирование наномолекулярных и ретикулярных архитектур с помощью программируемых дисков с шестигранной канавкой. J Chem Educ. 2020; 97 (1): 289–294. DOI: 10.1021 / acs.jchemed.9b00739. [CrossRef] [Google Scholar] 15. дель Кастильо П., Мейсон ПЛ. Биомолекулярное моделирование проволокой, ПВХ и пластилином: дешевая и универсальная система для использования в классе.Biochem Educ. 1997. 25 (1): 35–38. DOI: 10.1016 / S0307-4412 (96) 00129-X. [CrossRef] [Google Scholar] 16. Гонсалес-Санчес А.М., Ортис-Ньевес Е.Л., Медина З. Практическая деятельность, включающая тройное представление ограничивающего реагента. J Chem Educ. 2014. 91 (9): 1464–1467. DOI: 10.1021 / ed4003783. [CrossRef] [Google Scholar] 17. Дин Н.Л., Юэн С., Брейден Д., МакИндо Дж. С.. Наборы лазерных моделей с открытым исходным кодом для преподавания молекулярной геометрии. J Chem Educ. 2019; 96 (3): 495–499. DOI: 10.1021 / acs.jchemed.8b00553.[CrossRef] [Google Scholar] 18. Фурчес Д., Федуция Дж. Работа с трехмерной печатью под руководством студентов на курсах больших лекций: практическое руководство. J Chem Educ. 2018; 96 (2): 291–295. DOI: 10.1021 / acs.jchemed.8b00346. [CrossRef] [Google Scholar] 19. Савченков А.В. Разработка трехмерных моделей, которые можно распечатать по запросу и использовать со студентами для облегчения обучения молекулярной структуре, симметрии и связанным темам. J Chem Educ. 2020; 97 (6): 1682–1687. DOI: 10.1021 / acs.jchemed.0c00192. [CrossRef] [Google Scholar] 20.Скальфани В.Ф., Вайд Т.П. Трехмерные печатные молекулы и расширенные твердотельные модели для обучения симметрии и точечным группам. J Chem Educ. 2014. 91 (8): 1174–1180. DOI: 10.1021 / ed400887t. [CrossRef] [Google Scholar] 21. Дикенсон CE, Blackburn RAR, Britton RG. Мероприятие в мастерской по 3D-печати, которое помогает представлению молекул и пониманию учащимися формы и хиральности. J Chem Educ. 2020; 97 (10): 3714–3719. DOI: 10.1021 / acs.jchemed.0c00457. [CrossRef] [Google Scholar] 23. Ма И-З, Ян З-Л, Ван И, Ван Х-Х, Тиан СДж.Использование силиконовых шариков, встроенных в магнит, для создания стабильных моделей плотноупакованных кристаллических структур. J Chem Educ. 2020; 97 (11): 4063–4068. DOI: 10.1021 / acs.jchemed.0c00515. [CrossRef] [Google Scholar] 24. Seshadri K, Liu P, Koes DR. Учебная среда 3Dmoljs: система реагирования в классе для трехмерных химических структур. J Chem Educ. 2020; 97 (10): 3872–3876. DOI: 10.1021 / acs.jchemed.0c00579. [CrossRef] [Google Scholar] 25. Фатема А., Расул С., Хабиб У. Интерактивная трехмерная визуализация диаграмм химической структуры, встроенных в текст, для помощи в процессе пространственного обучения студентов.J Chem Educ. 2020; 97 (4): 992–1000. DOI: 10.1021 / acs.jchemed.9b00690. [CrossRef] [Google Scholar] 26. Грубер С., Джеймс А., Берхтольд Дж. Т., Вуд З. Дж., Скотт Г. Э., Алгул З. Инструмент визуализации интерактивных элементарных ячеек для структур кристаллической решетки. J Chem Educ. 2020; 97 (7): 2020–2024. DOI: 10.1021 / acs.jchemed.9b01207. [CrossRef] [Google Scholar] 28. Моралес-Видалес Дж. А., Сандовал Салазар С. А., Якобо-Фернандес Дж. М., Тлахуис-Флорес А. Платоновы тела и их программирование: геометрический подход. J Chem Educ. 2020; 97 (4): 1017–1025.DOI: 10.1021 / acs.jchemed.9b00751. [CrossRef] [Google Scholar] 29. Купер Р., Казанова Дж. Отображение двумерных атомных и молекулярных орбиталей с использованием системы Mathematica. J Chem Educ. 1991. 68 (6): 487–488. DOI: 10.1021 / ed068p487. [CrossRef] [Google Scholar] 30. D’Ambruoso GD, Cremeens ME, Hendricks BR. Интерактивные анимированные учебные пособия с использованием программного обеспечения для создания снимков экрана для молекулярного моделирования, а также для получения и обработки спектральных данных. J Chem Educ. 2018; 95 (4): 666–671. DOI: 10.1021 / acs.jchemed.7b00511. [CrossRef] [Google Scholar] 31.Хаворт Н.Л., Мартин Л.Л. Биомолекулы оживают: компьютерный лабораторный эксперимент для студентов-химиков. J Chem Educ. 2018; 95 (12): 2256–2262. DOI: 10.1021 / acs.jchemed.7b00931. [CrossRef] [Google Scholar] 32. Hanwell MD, Curtis DE, Lonie DC, Vandermeersch T, Zurek E, Hutchison GR. Avogadro: расширенный семантический химический редактор, платформа для визуализации и анализа. J Cheminformatics. 2012; 4 (1): 17. DOI: 10.1186 / 1758-2946-4-17. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 33. О’Брайен М.Создание трехмерных молекулярных моделей, чтобы помочь студентам визуализировать стереоселективные реакции. J Chem Educ. 2016; 93 (9): 1663–1666. DOI: 10.1021 / acs.jchemed.6b00250. [CrossRef] [Google Scholar] 34. Акуна В.В., Хоппер Р.М., Йодер Р.Дж. Компьютерный дизайн лекарств для лаборатории органической химии с использованием доступных инструментов молекулярного моделирования. J Chem Educ. 2020; 97 (3): 760–763. DOI: 10.1021 / acs.jchemed.9b00592. [CrossRef] [Google Scholar] 35. Allouche A-R. Gabedit — графический пользовательский интерфейс для программного обеспечения вычислительной химии.J. Comput Chem. 2011. 32 (1): 174–182. DOI: 10.1002 / jcc.21600. [PubMed] [CrossRef] [Google Scholar] 37. Полузащитник JE, Янсма AL. PyMOL как учебный инструмент для представления и управления белковой системой миоглобин / гемоглобин. J Chem Educ. 2019; 96 (11): 2540–2544. DOI: 10.1021 / acs.jchemed.9b00143. [CrossRef] [Google Scholar]38. Шмидт Дж. Р., Полик В. Ф. WebMO Enterprise. 20.0 изд. Голландия, Мичиган, США: WebMO LLC; 2020. 40. Петерсон С.Н., Тавана С.З., Акинли О.П., Джонсон В.Х., Беркмен МБ. Идея для изучения: использование дополненной реальности для обучения трехмерным биомолекулярным структурам.Биохим Мол Биол Образов. 2020; 48 (3): 276–282. DOI: 10.1002 / bmb.21341. [PubMed] [CrossRef] [Google Scholar] 41. Дай Р., Лауреанти Я.А., Копелевич М., Диаконеску П.Л. Разработка подхода виртуальной реальности для лучшего понимания координационной химии и молекулярных орбиталей. J Chem Educ. 2020; 97 (10): 3647–3651. DOI: 10.1021 / acs.jchemed.0c00469. [CrossRef] [Google Scholar] 42. Эриксен К., Нильсен Б.Е., Питтелькоу М. Визуализация трехмерных молекулярных структур с помощью приложения дополненной реальности. J Chem Educ. 2020; 97 (5): 1487–1490.DOI: 10.1021 / acs.jchemed.9b01033. [CrossRef] [Google Scholar] 43. Aw JK, Boellaard KC, Tan TK, Yap J, Loh YP, Colasson B и др. Взаимодействие с трехмерными молекулярными структурами с помощью мобильного приложения дополненной реальности. J Chem Educ. 2020; 97 (10): 3877–3881. DOI: 10.1021 / acs.jchemed.0c00387. [CrossRef] [Google Scholar] 44. Овенс М., Эллиард М., Хокинс Дж., Спаньоли Д. Разработка приложения дополненной реальности в студенческом эксперименте по преципитации ДНК, чтобы связать макроскопические и субмикроскопические уровни химии.J Chem Educ. 2020; 97 (10): 3882–3886. DOI: 10.1021 / acs.jchemed.0c00481. [CrossRef] [Google Scholar] 45. Маврикиос Д., Алексопулос К., Георгулиас К., Макрис С., Михалос Г., Хриссолурис Г. Использование голограмм для визуализации образовательного контента и взаимодействия с ним на учебной фабрике. Methodia Manuf. 2019; 31: 404–410. DOI: 10.1016 / j.promfg.2019.03.063. [CrossRef] [Google Scholar] 46. Хегарти М. Пространственное мышление в бакалавриате естественнонаучного образования. Spat Cogn Comput. 2014. 14 (2): 142–167. DOI: 10.1080 / 13875868.2014. 889696. [CrossRef] [Google Scholar] 47. Паниагуа Дж.К., Мота Ф., Соле А., Виласека Э. Лаборатория квантовой химии дома. J Chem Educ. 2008. 85 (9): 1288–1290. DOI: 10.1021 / ed085p1288. [CrossRef] [Google Scholar] 48. Олив Дж., Риффонт Д. Лаборатория квантовой химии дома: альтернатива Microsoft Windows. J Chem Educ. 2009; 86 (5): 567. DOI: 10.1021 / ed086p567.1. [CrossRef] [Google Scholar] 49. Дженсен Дж. Х., Кроман Дж. К.. Калькулятор молекул: веб-приложение для быстрой оценки свойств молекул на основе квантовой механики.J Chem Educ. 2013. 90 (8): 1093–1095. DOI: 10.1021 / ed400164n. [CrossRef] [Google Scholar] 50. Limpanuparb T, Sathainthammanee D, Pakwilaikiat P, Kaewpichit C, Yimkosol W, Suwannakhan A. Переосмысление популярных демонстраций для использования в лабораторных сеансах безопасности, которые вовлекают студентов в наблюдение, прогнозирование, ведение записей и решение проблем. J Chem Educ. 2021. 98 (1): 191–197. DOI: 10.1021 / acs.jchemed.9b00474. [CrossRef] [Google Scholar] 51. Limpanuparb T, Datta S, Chinsukserm K, Teeraniramitr P. In silico геометрические и энергетические данные всех возможных простых ротамеров, изготовленных из неметаллических элементов.Краткий обзор данных. 2020; 30: 105442. DOI: 10.1016 / j.dib.2020.105442. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 52. Суваннакхан А., Лимпанупарб Т. Задания по написанию Википедии: годичная пилотная программа на уроках химии в Университете Махидол. Катализатор. 2017; 16 (2): 65–79. [Google Scholar]Строительные блоки материи | АтомыЕсть только два класса чистых веществ, а именно элементов и соединений . Чтобы понять разницу между ними, взгляните на две диаграммы ниже. На диаграмме слева представлен элемент. Вы видите, что все атомы одного вида? Элемент — это материал, состоящий из атомов только одного вида. Теперь посмотрите на диаграмму справа, представляющую комплекс. На этой диаграмме показаны две важные вещи о соединениях: Соединение — это материал, состоящий из двух или более атомов, которые химически связаны друг с другом. Теперь мы рассмотрим каждый из этих классов отдельно и обсудим несколько примеров каждого из них. ЭлементыМы только что узнали, что элемент состоит из атомов одного вида. Это означает, что если бы у нас был кусок металлической меди, он бы полностью состоял из атомов меди. Точно так же кусок серебра будет полностью состоять из атомов серебра. Медь и серебро выглядят по-разному и имеют разные свойства, потому что состоят из разных атомов. Взгляните на следующую таблицу, которая иллюстрирует субмикроскопическое изображение атомов, а также ювелирное изделие, сделанное из каждого из различных металлов. ВОПРОСЫ: Почему атомы серебра больше, чем атомы меди на предыдущих диаграммах? Подсказка: найдите два элемента в Периодической таблице и сравните их положение.Серебро находится ниже меди в Периодической таблице, что означает, что атомы серебра больше, чем атомы меди.
Не важно, чтобы учащиеся ответили на этот вопрос; он предназначен для введения понятия, что оба элемента и соединения могут существовать как молекулы, но что молекулы элементов фундаментально отличаются от молекул соединений. Кластеры атомов в предыдущем примере называются молекулами. Молекула — очень важное слово в химии. Молекула — это два или более атома, которые химически связаны друг с другом. Атомы в молекуле могут быть одного типа (в этом случае это может быть молекула элемента) или они могут быть разных типов (в этом случае это может быть молекула соединения). Не все элементы имеют молекулы. Металлы в левой и средней части Периодической таблицы представляют собой твердые тела при комнатной температуре, поэтому они существуют в виде плотно упакованных массивов атомов, как в предыдущих примерах серебра и меди. Многие неметаллы в правой части Периодической таблицы представляют собой газы при комнатной температуре, которые существуют в виде молекул, состоящих из двух атомов каждая. Их называют двухатомными молекулами .Изображение элемента, которое мы обсуждали ранее, показывает, как выглядят двухатомные молекулы. Кислород (O 2 ), азот (N 2 ), водород (H 2 ), хлор (Cl 2 ) и некоторые другие элементы из неметаллов — все они образуют двухатомные молекулы. Нарисуйте изображение одной из этих двухатомных молекул в пространстве ниже. Учащиеся должны нарисовать два соединенных друг с другом круга одинакового размера и цвета.Предлагается научить учащихся создавать некоторые из двухатомных молекул с помощью бусинок, шариков из пластилина и т. Д. Убедитесь, что они знают, что бусинки теперь представляют собой целые атомы, а не субатомные частицы. Двухатомный относится к молекуле, состоящей из двух одинаковых атомов, связанных вместе, как в кислороде (O 2 ). «Ди» означает два. Трехатомный относится к молекуле, состоящей из трех одинаковых атомов, связанных вместе, как у озона (O 3 ). Это краткий обзор того, что учащиеся только что узнали об атомах и молекулах, и возможность различать их. Давайте удостоверимся, что мы понимаем разницу между атомами и молекулами. ВОПРОСЫ: Посмотрите на следующие схемы.Решите, представляет ли каждый из них атом или молекулу. Если это молекула, укажите, сколько атомов составляет молекула.
Теперь давайте подумаем об этом: если соединения состоят из двух или более видов атомов, это будет означать, что соединения состоят из двух или более различных элементов, которые объединились. СоединенияПо мере того, как вы читаете этот материал, предложите учащимся создавать свои собственные молекулы, используя бусинки или пластилин на столе перед ними. В известной нам Вселенной как минимум 118 элементов. Они могут образовывать соединения, связываясь в миллионы различных комбинаций — слишком много, чтобы обсуждать здесь! Мы рассмотрим несколько простых комбинаций элементов, чтобы проиллюстрировать идею. Поскольку вода является таким важным компонентом для организмов, живущих на Земле, мы будем использовать это в качестве нашего первого примера. Ученые знают, что молекула воды состоит из одного атома кислорода и двух атомов водорода. Если бы мы могли их увидеть, все молекулы воды были бы немного похожи на эту диаграмму молекулы воды. Представление молекулы воды.Международный союз теоретической и прикладной химии (IUPAC) называет воду монооксидом дигидрогена. Все молекулы воды абсолютно одинаковы. Мы говорим, что атомы связаны в фиксированном соотношении : два атома водорода на каждый атом кислорода. Атомы в молекуле удерживаются вместе особой силой, которую мы называем «химическая связь ». Эти связи известны как ковалентные связи, но учащиеся пока не обязаны это знать. На этом этапе вы также можете напомнить учащимся, что диаграммы молекул — это просто представления, и мы используем разные цвета, чтобы различать атомы разных элементов.Атомы кислорода на самом деле не красные. Химические формулыМожете ли вы вспомнить, что у каждого элемента есть свой уникальный химический символ? Мы можем объединить эти символы в химическую формулу воды. Химическая формула — еще одно очень важное понятие в химии. Химическая формула воды: H 2 O. Она показывает отношение атомов водорода (два) к атомам кислорода (один) в одной молекуле воды.Как вы думаете, о чем нам говорит химическая формула CO 2 ? Он говорит нам, что один атом углерода (C) связан с двумя атомами кислорода (O) в CO 2 . На этом этапе предлагается написать несколько химических формул на доске и попросить учащихся объяснить вам, что каждый из них говорит вам. Попросите учащихся делать заметки на боковых полях своих рабочих тетрадей, пока вы обсуждаете это в классе. Это послужит введением к следующему занятию.Например, вы также можете написать:
В следующем упражнении мы попрактикуемся в написании и понимании химических формул. Всегда полезно думать о новой концепции разными способами. По этой причине мы также собираемся построить модели молекул, для которых пишем формулы. МАТЕРИАЛЫ:
ИНСТРУКЦИЯ:
Чтобы помочь вам в этом, вот несколько рекомендаций:
На этом этапе не важно, чтобы учащиеся правильно знали точные углы между атомами, такие как угол между атомами водорода в молекуле воды, поскольку они узнают только о том, что влияет на это позже в Gr.10-12.
Заполненная таблица должна выглядеть следующим образом.
ВОПРОСЫ: Перечислите все вещества из таблицы, которые являются элементами.Напишите их имена и формулы.Водород, H 2 Кислород, O 2 Хлор, Cl 2 Азот, N 2 Перечислите все вещества из таблицы, которые являются соединениями.Напишите их имена и формулы.Вода, H 2 O Двуокись углерода, CO 2 Диоксид серы, SO 2 Натрия хлорид, NaCl Сероводород, H 2 S Аммиак, NH 3 Как вы узнали, какие вещества в таблице являются соединениями, а не элементами? Вы, вероятно, искали, чтобы увидеть, какие из них состоят из более чем одного вида атомов.Соединение — это материал, состоящий из атомов двух или более различных элементов. Элементы не просто смешаны физически, но химически связаны друг с другом на атомном уровне. Вода (H 2 O), диоксид углерода (CO 2 ) и соль или хлорид натрия (NaCl) являются примерами соединений, в то время как газообразный кислород (O 2 ), газообразный водород (H 2 ) и газообразный азот (N 2 ) являются примерами элементов. Соединение формулы H 2 O 2 также состоит из атомов водорода и кислорода.Формула говорит нам, что одна молекула этого вещества состоит из двух атомов водорода и двух атомов кислорода. H 2 O 2 то же самое, что вода? Как вы думаете? Не путайте H 2 O 2 с H 2 O! H 2 O 2 представляет собой соединение, называемое пероксидом водорода. Перекись водорода похожа на воду в том, что при комнатной температуре (25 ° C) это прозрачная бесцветная жидкость, хотя и не такая жидкая, но во многом отличается.Следующие свойства перекиси водорода могут убедить вас в том, что это не то же самое, что вода:
Коррозионные вещества — это вещества, которые вызывают повреждение металла или других материалов в результате химического процесса. Представьте, что дождевая вода вызывает ржавчину, разъедающую металл. Если это вас не убеждает, давайте сравним, как выглядит молекула перекиси водорода рядом с водой: Перекись водорода. Вода.Несмотря на то, что они состоят из одних и тех же элементов, эти два соединения очень разные, и их никогда не следует путать друг с другом. Целью приведенного выше сравнения перекиси водорода и воды было показать вам, что атомы в данном соединении всегда соединяются в фиксированном соотношении. Во всех молекулах воды во Вселенной всегда будет один атом O и два атома H, связанные вместе. Это был пятый постулат Далтона: 5. Атомы химически соединяются в фиксированных соотношениях с образованием соединений. Как атомы «сочетаются»? Что заставляет их слипаться и образовывать молекулы? Химические связиВзгляните на фото с различным расположением металлических шариков. Эти шарики магнитные, и это позволяет вам создавать разные узоры, склеивая их вместе. Что заставляет магниты склеиваться? Учащиеся могут сказать, что магниты слипаются, потому что они притягивают друг друга.Укажите им, что магниты действительно будут притягиваться друг к другу, если они выстроены правильно. Магниты также могут отталкивать друг друга, если они расположены по-другому. Учащиеся будут больше изучать магнитные силы в Gr. 9 Энергия и перемены. Эти шары магнитные. http://www.flickr.com/photos/uscpsc/6331652875/Магниты притягивают (или отталкивают) друг друга из-за магнитной силы между ними (вы узнаете больше о магнитах в Gr.9). Когда атомы объединяются, они делают это, потому что они также испытывают силу притяжения. Сила немного сложнее, чем сила между магнитами, но работает она так же: сила удерживает атомы вместе, как будто они склеены клеем. Силы, удерживающие атомы вместе, называются химическими связями . В молекуле воды химические связи между O и двумя атомами H удерживают всю молекулу вместе. Сколько химических связей в каждой молекуле воды? Если вы не уверены, посмотрите на диаграмму ниже: Две облигации.Если вы хотите вывести учащихся за рамки требований учебной программы на данном этапе, вы могли бы дать краткое объяснение электронного обмена. Детали этого будут изучены только в Gr. 10. Эти прочные химические связи, называемые ковалентными связями, образуются, когда атомы делятся своими электронами. Это объясняет, почему после реакции разложения атомы немедленно преобразуются во что-то еще: требование совместного использования электронов, которое привело к исходной связи, все еще существует, они просто разделяют электроны с другим атомом. Молекула воды имеет две идентичные связи O-H. Что бы произошло, если бы у нас было достаточно энергии, чтобы разорвать эти узы? Если бы у нас было достаточно энергии, чтобы разорвать связи O-H, мы смогли бы отделить атомы друг от друга. Что было бы, если бы мы разделили молекулы воды на их атомы? Теоретически у нас были бы атомы водорода и кислорода.На самом деле происходит то, что атомы водорода немедленно объединяются с образованием H 2 , а атомы кислорода немедленно объединяются с образованием O 2 . Когда атомы отделяются друг от друга и рекомбинируют в различные комбинации атомов, мы говорим, что произошла химическая реакция . В ходе указанной выше химической реакции вода разложилась (распалась) и рекомбинировала на более мелкие молекулы.Мы говорим, что вода подверглась реакции разложения в приведенном выше примере. Конечно, не все химические реакции являются реакциями разложения. Существует много различных видов химических реакций, и мы собираемся исследовать некоторые примеры в следующем разделе. Химические реакцииВо всех химических реакциях происходят два важных события:
Это означает, что в всех химических реакциях атомы в молекулах перестраиваются, образуя новые молекулы. В следующем упражнении мы собираемся смоделировать реакцию разложения воды, используя глину или шарики из пластилина для представления различных атомов. Это дополнительное расширение. Позднее в семестре учащиеся будут больше изучать химические реакции. МАТЕРИАЛЫ:
ИНСТРУКЦИЯ:
Можете ли вы написать химическое уравнение реакции, которую вы только что построили, с помощью глиняных моделей? Посмотрите на схему для вдохновения: 2 H 2 O \ (\ rightarrow \) 2 H 2 + O 2 Химические уравнения будут правильно представлены в последней главе Gr.8 Материя и материалы, но это может быть хорошим местом, чтобы начать привлекать к этому внимание учащихся. Вы могли бы объяснить, что когда есть только одна молекула определенного типа (O 2 в приведенном выше примере), мы не пишем число перед ней в химической реакции. На данном этапе балансировка уравнений не требуется. Давайте посмотрим на другой пример химической реакции: реакция, когда углерод (в угле) реагирует с кислородом (в воздухе) с образованием диоксида углерода: Вы можете использовать шарики из пластилина, чтобы имитировать эту реакцию. Попытайтесь написать химическое уравнение реакции, когда углерод и кислород соединяются с образованием диоксида углерода. (Подсказка: используйте диаграмму, чтобы направлять вас.) C + O 2 \ (\ rightarrow \) CO 2 Как атомы угля и кислорода перегруппировываются с образованием диоксида углерода? Какая связь рвется? Связь между двумя атомами кислорода разрывается. Какие новые облигации образуют? Две новые углеродно-кислородные связи образуются при образовании диоксида углерода. Затем ваш учитель продемонстрирует классу две химические реакции.Ваша задача — внимательно наблюдать и записывать свои наблюдения, которые вы можете видеть в происходящем. Мы предлагаем сделать это в качестве демонстрации или провести несколько экспериментов в классе, за которыми могут наблюдать разные группы учащихся. Видео в окне для посещения содержит простую демонстрацию электролиза с использованием сульфата меди вместо хлорида меди. Но наблюдения будут такими же, а именно, что металлическая медь покрывает катод, и вы можете наблюдать пузырьки газа на аноде (на видео это газообразный кислород, а не газообразный хлор, как в исследовании здесь, в рабочей тетради. Видео, демонстрирующее аналогичную реакцию с использованием сульфата меди. AIM: Определить, можно ли разложить хлорид меди с помощью электроэнергии. МАТЕРИАЛЫ И АППАРАТ:
Вместо графитовых электродов можно также получить угольные электроды из использованных ячеек горелки. Длина провода с зажимами типа «крокодил» на обоих концах является идеальной. Они понадобятся вам для построения электрической цепи. Включение переключателя в схему не является обязательным. Раствор хлорида меди можно приготовить, растворив две чайные ложки хлорида меди (II) в стакане водопроводной воды. Перед запуском сделайте следующие наблюдения: Какого цвета раствор хлорида меди?Какого цвета графитовые электроды? МЕТОД:
НАБЛЮДЕНИЯ: Что вы наблюдаете на поверхности двух электродов после того, как реакция продолжалась в течение нескольких минут?Один электрод покрывается маленькими пузырьками, а другой становится коричневым. Какого цвета в конце эксперимента был хлорид меди?Решение все еще синее. Если вы сохранили часть исходного решения, учащиеся могут сравнить решение до и после эксперимента.Они могут заметить, что решение «после» не такое синее, как решение «до». Попросите учащихся задуматься, почему это могло быть. Это связано с двумя причинами:
Следовательно, , концентрация раствора хлорида меди становится слабее, в результате чего он становится немного менее синим. Как изменился внешний вид графитовых электродов?Один электрод остается темно-серым или черным.Другой электрод покрыт красновато-коричневым слоем. Можно отметить, что электрод, который остался серо-черным, был тем же электродом, на котором раньше были пузырьки. Попросите учащихся почувствовать запах этого электрода. Они могут чувствовать запах отбеливателя, который представляет собой запах газообразного хлора Cl 2 . Попросите учащихся сравнить цвет слоя с цветом медной монеты.Может ли налет на втором электроде быть медью? Да, это. Учащимся не нужно понимать, что происходит в растворе на ионном уровне. Акцент здесь делается на демонстрации того, что соединение можно разбить на элементы. Тем не менее, объяснение электролиза раствора хлорида меди (II) приводится здесь для справки, и если вы хотите расширить свои знания учащихся:
(Вы можете попросить учащихся нарисовать положительные и отрицательные знаки и пометить электроды на диаграммах в своих рабочих тетрадях в качестве расширения.) Электрод, прикрепленный к положительной стороне батареи, является положительным электродом и называется анодом .Электрод, прикрепленный к отрицательной стороне батареи, является отрицательным электродом и называется катодом . Обобщите ваши экспериментальные наблюдения в следующей таблице.
АНАЛИЗ И ОБСУЖДЕНИЕ: Что придало раствору хлорида меди насыщенный синий цвет?Растворенный в нем хлорид меди. Как вы думаете, часть хлорида меди могла измениться во время реакции во что-то другое? Объясните, почему вы так думаете.Раствор хлорида меди стал менее голубым. Это говорит нам о том, что часть хлорида меди превратилась во что-то другое. Как бы вы объяснили появление пузырьков на поверхности первого электрода? Вы хоть представляете, какими они могли быть? Подсказка: чем пахнет электрод потом?Пузырьки означают, что на поверхности электрода образовался газ.Пахло отбеливателем. Газообразный хлор также пахнет отбеливателем, поэтому возможно, что газ, образующийся на электроде, мог быть хлором. Примечание: Хлор фактически является активным ингредиентом отбеливателя. Вы знаете, что такое красновато-коричневый налет на втором электроде? Подсказка: какой металл имеет такой же характерный красновато-коричневый цвет?Возможно, красновато-коричневый налет — это медь. Как мы узнаем, что произошла химическая реакция?Атомы в хлориде меди были перегруппированы, чтобы образовать различные материалы: медь (Cu) и хлор (Cl 2 ). ВЫВОД: Напишите заключение для расследования.В своем заключении вам следует переписать цель расследования в изложение результатов вашего расследования.Заключение обучаемого должно содержать как минимум два из следующего: Как вы думаете, возможно ли разделить хлорид меди на медь и хлор с помощью любого из методов физического разделения, о которых мы узнали в Gr.7 Материя и материалы, такие как просеивание, фильтрация, выпаривание, дистилляция или хроматография? Вот подсказка: ни один из этих методов не может разорвать связи между атомами в веществе. Ответ — нет. Медь и хлор химически связаны в хлориде меди. Мы знаем это из его химической формулы: CuCl 2 . Методы физического разделения могут использоваться только для разделения смесей на вещества, из которых они состоят. На данный момент мы узнали об атомах, молекулах, элементах и соединениях. Иногда эти концепции сбивают с толку, потому что они описывают вещи, которые слишком малы, чтобы их можно было увидеть, а иногда и трудно представить. В следующем разделе мы вернемся к идее смесей и посмотрим, как все, что мы узнали до сих пор, можно поместить в схему классификации материи и материалов. Создание молекулярной моделиВо время этого упражнения мы собираемся использовать легкодоступные материалы, которые мы все можем найти дома или легко купить в супермаркете, чтобы создать молекулярную модель молекулы аромата.Мы хотели бы, чтобы вы попробовали сделать пропилэтаноат (CH 3 CO 2 CH 2 CH 2 CH 3 ), и мы хотим, чтобы вы проявили как можно более творческий подход к материалам, которые вы использовать! Но помните, что мы по-прежнему хотим иметь возможность увидеть истинное представление молекулы (т.е. чтобы она имела правильную трехмерную форму со связанными углами, которые выглядят достаточно точными). Потребуются следующие ингредиенты:
Шаг первый: выберите свою ароматическую молекулуМы сделали попытку воссоздать сложный эфир, который мы хотели бы, чтобы вы сделали (пропилэтаноат) — скелетная структура показана ниже.Шаг второй: выберите материалыДля наших молекул мы решили использовать красные мармеладные конфеты для кислорода, черные мармеладные конфеты для углерода, белые мини-маршмеллоу для водорода и коктейльные палочки для связующих.Но именно здесь вы можете проявить себя по-настоящему творчески! Вы можете использовать фрукты, марципан, пластилин… все, что у вас есть в доме, что может работать как атомы и молекулы — мы оставим эту сторону вещей на ваше усмотрение.Шаг третий: попробуйтеВот изображение нашего липкого сладкого творения! Может быть довольно сложно заставить модели стоять вертикально, но главное, вы можете использовать свою модель, чтобы визуализировать молекулы аромата в 3D. Чтобы обеспечить стабильность, для некоторых одинарных связей в нашем творении жевательной конфеты потребовались две коктейльные палочки, расположенные рядом друг с другом — для двойной связи коктейльные палочки хорошо разделены с очевидным зазором между ними.Если вы застряли, пытаясь создать свою молекулярную модель, ознакомьтесь с нашими советами и подсказками в формате pdf в разделе загрузок ниже. Это дает пошаговое руководство, которое может быть полезно при попытке получить правильные валентные углы вокруг ваших атомов. Когда вы закончите, мы будем рады увидеть ваши творческие шедевры! Почему бы не загрузить изображение вашей модели в нашу открытую Padlet (мы включили несколько примеров из предыдущих курсов, чтобы вдохновить вас) или использовать Twitter или Instagram #FLchemistry, чтобы рассказать, как у вас дела.Кроме того, дайте нам знать, как вы справились с задачей, используя раздел комментариев ниже. Если вам нужны какие-либо инструкции по использованию Padlet, тогда доступна дополнительная информация — мы очень хотели бы, чтобы каждый почувствовал себя частью обучающегося сообщества, поэтому с нетерпением ждем ваших отзывов. Для вашей безопасности рекомендуется не употреблять в пищу какие-либо части созданной вами молекулярной модели на любом этапе эксперимента (негигиеничное обращение с пищевыми продуктами может привести к заражению). Выбросьте образцы в мусорную корзину. Примите соответствующие меры при использовании коктейльных палочек или других острых предметов, чтобы не пораниться.Конкурс моделейБудет разыгран приз за фотографию лучшей модели пропилэтаноата, размещенную на нашем сайте Padlet и / или в Twitter или Instagram до 9:00 понедельника 6 июля (неделя 2) . Приз будет вручен моделисту, модель которого, по мнению Энди, является самой оригинальной, яркой, творческой и научно точной.Мы объявим имя победителя на второй неделе (в комментариях ниже), которому будут отправлены потрясающие бутылки с водой Chemistry @ York и спиннер . (Этот конкурс проводится Энди из Йоркского университета и не связан с FutureLearn, и любые личные данные, предоставленные учащимся, будут использоваться только для отправки приза.) Почему бы не попробовать?Движение частицЭта идея фокусировки исследуется через: Противопоставление взглядов студентов и ученыхЕжедневный опыт студентовНа этом уровне студенты должны «объяснять поведение и свойства материалов с точки зрения составляющих их частиц и сил, удерживающих их вместе» (стандарты VELS, уровень 6).Однако тот факт, что учащиеся могут рисовать обычные статические расположения частиц в твердых телах, жидкостях и газах, не означает, что они придерживаются полного представления о материи. Исследования показывают, что многие студенты в этом возрасте и старше все еще придерживаются ряда альтернативных представлений о частицах, которые трудно погасить. Они часто не осознают очень маленький размер частиц, приписывают микроскопическим частицам макроскопические свойства, испытывают трудности с пониманием движения частиц во всех состояниях материи и имеют проблемы с пониманием сил между частицами. Research: Driver (1987) Многие студенты, которые понимают, что материя представляет собой твердые частицы, все еще сохраняют прежние взгляды и считают, что частицы могут изменять свою форму (от твердого до жидкого), взрываться, гореть, расширяться, изменять форму и цвет или сжиматься. Студенты визуализируют атомы, молекулы и ионы как маленькие шарообразные объекты (возможно, из-за способа представления информации), и это способствует тому, что они путают свойства частиц с макроскопической природой материалов, из которых они состоят. Research: Happs (1980) Эти идеи также рассматриваются в идее фокуса. Макроскопические и микроскопические свойства. Студенты часто не понимают динамическую природу частиц; они склонны думать о них как о статичных. Студенты могут верить, что частицы газа движутся медленно, подобно тому, как они наблюдают, когда видят взвешенные частицы пыли в луче света. Случайное движение частиц в жидкостях и газах — трудная для понимания концепция.На вопрос: «Почему частицы газа не падают на дно сосуда?» только около 50% студентов думали, что частицы находятся в постоянном движении. Студенты заявили, что частицы раздвигались (под действием тепла, действующего как вещество) при нагревании газов. Когда газы конденсировались в жидкость, многие студенты объясняли это увеличением сил притяжения между частицами. Исследования: Новик и Нуссбаум (1981) Студентам часто трудно оценить движение частиц в твердых телах, и это приводит к различным представлениям о замораживании и плавлении.Вот несколько примеров того, как студенты думают о поведении частиц в тающей ледяной глыбе: Студент 1: «Частицы начинают отламываться друг от друга из-за повышения температуры. Когда они отделяются друг от друга, они превращаются из кристаллической формы в форму раствора ». Студент 2:« Когда кусок льда вынимается из морозильника, резкое изменение температуры реагирует на частицы, заставляющие их уменьшиться в размерах ». Scientific viewАтомы невероятно малы, и их невозможно увидеть даже с помощью самого мощного светового микроскопа.Мы используем несколько моделей атомов, чтобы объяснить химические процессы и описать их поведение. В газах частицы быстро движутся во всех направлениях, часто сталкиваясь друг с другом и стенками контейнера. С повышением температуры частицы приобретают кинетическую энергию и движутся быстрее. Фактическая средняя скорость частиц зависит от их массы, а также от температуры — более тяжелые частицы движутся медленнее, чем более легкие, при той же температуре. Молекулы кислорода и азота в воздухе при нормальной комнатной температуре быстро перемещаются со скоростью от 300 до 400 метров в секунду.В отличие от столкновений между макроскопическими объектами, столкновения между частицами являются совершенно упругими без потери кинетической энергии. Это сильно отличается от большинства других столкновений, когда некоторая кинетическая энергия преобразуется в другие формы, такие как тепло и звук. Совершенно эластичный характер столкновений позволяет частицам газа продолжать отскакивать после каждого столкновения без потери скорости. Частицы по-прежнему подвержены силе тяжести и ударяются о дно контейнера с большей силой, чем о верх, что придает газу вес.Если бы вертикальное движение молекул газа не замедлялось под действием силы тяжести, атмосфера давно бы покинула Землю. В жидкостях частицы расположены довольно близко друг к другу и беспорядочно перемещаются по контейнеру. Частицы быстро движутся во всех направлениях, но сталкиваются друг с другом чаще, чем в газах, из-за более коротких расстояний между частицами. С повышением температуры частицы движутся быстрее, поскольку они набирают кинетическую энергию, что приводит к увеличению частоты столкновений и увеличению скорости диффузии. В твердом теле частицы упаковываются вместе настолько плотно, насколько это возможно, в аккуратном и упорядоченном расположении. Частицы удерживаются вместе слишком сильно, чтобы их можно было перемещать с места на место, но частицы действительно колеблются относительно своего положения в структуре. С повышением температуры частицы приобретают кинетическую энергию и вибрируют быстрее и сильнее. Сила притяжения в твердых телах не обязательно должна быть сильнее, чем в жидкостях или газах. Например, силы между твердыми частицами гелия (при -270 ° C) все еще очень слабы.Для сравнения, силы между частицами паров железа (требующие очень высоких температур) очень велики. Если вы сравните разные вещества, имеющие одинаковую температуру, то средняя кинетическая энергия частиц будет одинаковой (т. Е. Если частицы имеют одинаковую массу, они будут двигаться с одинаковой скоростью), но силы притяжения в твердых телах будут быть больше, чем в жидкостях, которые будут больше, чем в газах. Силы притяжения не ослабевают, когда вещество переходит из твердого состояния в жидкое, а затем в газообразное, скорее, кинетическая энергия частиц увеличивается (что подразумевает более быстрое движение), позволяя им преодолевать силы притяжения. Критические идеи обучения
Изучите взаимосвязь между идеями о движении частиц в Карты развития концепции — (химические реакции, состояния материи) Студенты этого уровня неоднократно сталкивались с идеями о частицах (включая атомы, ионы и молекулы), однако многие из них сохраняют альтернативные или наивные взгляды на природа частиц, и они могут препятствовать их пониманию.Стремитесь принять стратегии обучения, которые вызывают у учащихся неудовлетворенность их существующими идеями, и продвигать научную концепцию, которая будет правдоподобной, последовательной и полезной в различных ситуациях. Преподавательская деятельностьВыявите существующие идеи студентовВажно выяснить предыдущие взгляды большинства студентов в начале обучения, чтобы установить их существующее понимание модели частиц материи. Спросите студентов, что они думают о размере атомов по сравнению с другими мелкими объектами, такими как клетки, бактерии и вирусы.Это можно сделать, попросив их нарисовать их относительный размер в одном масштабе (шкале, где человеческая клетка равна размеру страницы или плаката). Выразите идею о том, что атомы снова стали намного меньше. Поищите другие занятия, которые помогут укрепить идею о том, что частицы очень и очень маленькие. Покажите студентам обычные рисунки частиц в твердых телах, жидкостях и газах и спросите их, движутся ли они и с какой скоростью. Бросить вызов существующим идеямЗдесь актуален ряд вопросов, поднятых в основной идее «Сохранение массы», и взвешивание колбы, содержащей небольшое количество ацетона до и после испарения, может быть использовано для проверки идей студентов. о том, что вещество легче в газовом состоянии, и о проблемах со статическими изображениями частиц газа в текстах.Для получения дополнительной информации см .: Сохранение массы. Помогите учащимся выработать для себя некоторые «научные» объясненияПри небольшом поощрении класс обычно может решить путем обсуждения, что частицы в газах должны падать на дно колбы сильнее, чем на верх, и, следовательно, на них действует сила тяжести. Это может быть расширено до объяснения того, почему атмосфера Земли истончается и в конечном итоге прекращается — вертикальное движение частиц вверх прекращается. Содействовать осмыслению и прояснению существующих идей и поощрять студентов к выявлению явлений, не объясненных (в настоящее время представленной) научной моделью или идеейПоскольку частицы нельзя наблюдать напрямую, большая часть обучения включает поиск очевидных проблем или несоответствий с своего рода статические изображения частиц, данные в предыдущие годы.Предложите студентам определить их и обсудить возможные объяснения. Некоторые подсказки:
Если необходимо, поднимите подобные вопросы, которые откроют дискуссию, но лучше, если учащиеся предложат некоторые из них сами. Обратите внимание, что многие проблемы связаны с газами — для объяснения именно их свойств нам больше всего нужна модель твердых частиц. Чтобы усилить понятие упругих столкновений, спросите, что произошло бы, если бы столкновения между частицами газа не были упругими. Какие практические последствия были бы для людей? Это можно представить, бросая различные типы мячей (например, футбольный мяч, мяч для настольного тенниса и надувной мяч (из магазинов игрушек)) и объясняя, что надувной мяч ведет себя больше как частицы газа. Начать обсуждение через общий опытИспользование таких упражнений, как POE (Прогнозировать-Наблюдать-Объяснять), может помочь учащимся задуматься, а затем подвергнуть сомнению свои существующие идеи.Следующее задание поможет учащимся обдумать свои представления о движении частиц. Установите две пары колб, каждая из которых соединена клапаном (см. Схемы ниже). Обе пары содержат коричневый диоксид азота в левой колбе.
Эксперименты по диффузии могут укрепить идею движения частиц.Их также можно использовать как POE. Например:
Броуновское движение также можно наблюдать с помощью стереомикроскопов, когда порошок серы или камфора разбрызгивается на поверхность воды или этанола. Практикуйтесь в использовании и создайте воспринимаемую полезность научной модели или идеиКусок ваты, пропитанный аммиаком, помещается на один конец длинной стеклянной трубки, а другой, пропитанный соляной кислотой (HCl), помещается на другой конец . В конце концов, на стыке двух газов образуется белое кольцо. Два газа имеют одинаковую температуру и, следовательно, частицы имеют одинаковую кинетическую энергию; кольцо образуется ближе к источнику более тяжелой и, следовательно, более медленно движущейся HCl.Это предсказывается сравнением относительных молекулярных масс. Наличие в трубке полоски универсальной индикаторной бумаги позволяет отслеживать диффузию газа. Это пример POE, в котором полезно привлечь внимание студентов к соответствующему разделу науки, прежде чем они сделают свой прогноз, поскольку он создает полезность для концепции относительной молекулярной массы (значений Mr). Студентам должна быть предоставлена возможность использовать научные концепции теории частиц в других условиях.Попросите учащихся понаблюдать, а затем объяснить изменения с точки зрения движения частиц в таких сценариях, как плавление воска или пластика, исчезновение нафталина в шкафу и запах духов, распространяющийся по комнате. моделей молекул из пластикового конструктора Фотография, картинки, изображения и сток-фотография без роялти. Изображение 99709235.моделей молекул из пластикового конструктора Фотография, картинки, изображения и сток-фотография без роялти. Изображение 99709235.Модели молекул из пластикового конструктора M L XLТаблица размеров
Используете это изображение на предмете перепродажи или шаблоне? Распечатать Электронный Всесторонний 3232 x 2100 пикселей | 27.4 см x 17,8 см | 300 точек на дюйм | JPG Масштабирование до любого размера • EPS 3232 x 2100 пикселей | 27,4 см x 17,8 см | 300 точек на дюйм | JPG Скачать Купить одно изображение 6 кредит Самая низкая цена
221 ру за изображение любой размер Цена денег Ключевые слова Похожие изображения Нужна помощь? Свяжитесь с вашим персональным менеджером по работе с клиентами @ +7 499 938-68-54 Мы используем файлы cookie, чтобы вам было удобнее работать.Используя наш веб-сайт, вы соглашаетесь на использование файлов cookie, как описано в нашей Политике использования файлов cookie . ПриниматьГлина в пластик | Университет штата ПенсильванияПластик дешевый. Это его ниша. Он дешевый и универсальный, поэтому его можно найти повсеместно. Но пластик, если говорить о нем, — вещь довольно посредственная. По сравнению, например, с металлом, — говорит Эвангелос Маниас, — полимеры обладают плохими материальными свойствами ». Эвангелос Маниас На протяжении десятилетий исследователи работали над улучшением этих свойств, добавляя к пластику «наполнители» — небольшие количества талька, стекла или углерода для придания прочности или упругости.Сейчас Маниас, доцент кафедры материаловедения и инженерии Пенсильванского университета, работает над новым типом добавки: натуральными глинами. Частицы глины, объясняет Маниас, чрезвычайно крошечные, от полмикрона до микрона в поперечнике и не более трех-пяти атомов толщиной. «Когда вы диспергируете эти частицы в полимере, — говорит Маниас, — они выглядят как крошечные листы бумаги». Взятые вместе, тысячи этих сверхтонких листов составляют большую площадь поверхности. И весь этот интерфейс оказывает большое влияние на свойства полимера. Автомобильная промышленность первой заметила этот эффект. «Около восьми лет назад Toyota стремилась улучшить термостойкость полимеров, чтобы производить более дешевые автомобильные детали, заменяя металлические и керамические корпуса пластиковыми», — говорит Маниас. «Они начали с нейлона 6», обычного промышленного полимера, который начинает размягчаться при 60 ° C. Когда к нейлону добавляли 3-5% глины, термостойкость композитного материала подскочила до 140 ° C — «достаточно хорошо, чтобы изготавливать детали. для под капотом.” Помимо сохранения прочности при высоких температурах, добавление глины улучшает барьерные свойства пластика, то есть его способность удерживать газы и жидкости или удерживать их. Этот эффект привлек внимание производителей упаковки для пищевых продуктов. По словам Маниуса, из глины можно сделать дешевые пластиковые бутылки, пригодные для хранения пива или вина. «Герметичная упаковка» также необходима внутри вашего компьютера, отмечает он. («Здесь кислород — не большая проблема, а вода. Вы же не хотите, чтобы эти чипсы намокали.») И внутри вашего тела тоже. В настоящее время Маниас работает с Джеймсом Рантом, профессором материаловедения и инженерии, и исследователями из Медицинского колледжа над улучшением полимеров, используемых для создания искусственного сердца штата Пенсильвания. Он отмечает, что принцип действия улучшенных барьерных свойств в этих «нанокомпозитах» не химический, а физический. «Когда вы добавляете глину, вы добавляете тысячи крошечных частиц, которые эти молекулы должны вращать», чтобы пройти через полимерную матрицу.Эта молекулярная полоса препятствий «повышает барьерные свойства как минимум в десять раз. А поскольку желаемый эффект зависит от размера частиц и площади поверхности, а не от химических реакций, глины можно использовать повсеместно. «Они не зависят от полимера. «То, что никто не предсказывал, — добавляет он, — это влияние диспергирования глины на огнестойкость». При сгорании полимеры сжимаются, а частицы глины внутри них стягиваются вместе, образуя обугленный, плотное уплотнение, подавляющее огонь. удерживая кислород.Таким образом, глина может быть более безопасной альтернативой применяемым в настоящее время антипиренам на основе брома, которые выделяют токсичные газы при горении. «Что больше всего волнует людей в индустрии пластмасс, так это то, что с помощью глин можно одновременно улучшить ряд свойств», — говорит Маниас. Прямо сейчас он и другие упорно трудятся, чтобы найти лучшие и самые дешевые рецепты для создания новых композитов. Глины и полимеры обычно не смешиваются, объясняет он: «Они как масло и вода». Один из подходов заключается в добавлении поверхностно-активных веществ непосредственно в глину. Этот процесс уже используется для смешивания глины с красками и косметикой.Другой сначала модифицирует полимер. По словам Маниаса, любой метод можно довольно легко включить в стандартное промышленное производство пластмасс. «Но это новая область. Мы все еще занимаемся фундаментальной химией и физикой ». Евангелос Маниас, доктор философии, доцент Филипа Уокера в области материаловедения и инженерии в Колледже наук о Земле и минералах, 325-D Steidle Bldg., University Park, PA 16802; 814-863-2980; [email protected]. Его работа поддерживается Национальным институтом стандартов и технологий, Национальным научным фондом, Национальными институтами здравоохранения и Федеральным авиационным управлением. . |


 Сразу сделать колбаску нужной длины сложно, но можно соединить друг с другом несколько коротких колбасок.
Сразу сделать колбаску нужной длины сложно, но можно соединить друг с другом несколько коротких колбасок. Еще проще сделать эту деталь из пенопластового яйца для поделок.
Еще проще сделать эту деталь из пенопластового яйца для поделок.
Leave a Reply