Молекула поваренной соли фото – Физические свойства поваренной соли 🚩 главные свойства поваренной соли 🚩 Естественные науки
Формула и свойства поваренной соли. Применение поваренной соли :: SYL.ru
Поваренная соль, формула которой NaCl, является пищевым продуктом. В неорганической химии данное вещество называют хлоридом натрия. В измельченном варианте поваренная соль, формула которой приведена выше, представляет собой белые кристаллы. Несущественные серые оттенки могут появляться при наличии иных минеральных солей в качестве примесей.
Производят ее в различных видах: неочищенном и очищенном, мелком и крупном, йодированном.

Биологическое значение
Кристалл поваренной соли, имеющий ионную химическую связь, необходим для полноценной жизни и деятельности человека, иных живых организмов. Хлорид натрия принимает участие в регулировании и поддержании водно-солевого баланса, щелочного обмена. Биологические механизмы контролируют постоянство концентрации хлористого натрия в различных жидкостях, например, в крови.
Разность концентраций NaCl внутри клетки и снаружи – основной механизм для попадания внутрь питательных веществ, а также вывода продуктов жизнедеятельности. Аналогичный процесс применяется в генерации и передаче нейронами импульсов. Также анион хлора в данном соединении – основной материл для образования соляной кислоты, важнейшего компонента желудочного сока.
Дневная потребность в этом веществе составляет от 1,5 до 4 граммов, а для жаркого климата доза хлорида натрия возрастает в несколько раз.
Организм нуждается не в самом соединении, а в катионе Na+ и анионе Cl-. При недостаточном количестве этих ионов происходит разрушение мышечной и костной тканей. Появляются депрессии, психические и нервные заболевания, нарушения в деятельности сердечно-сосудистой системы и процессах пищеварения, спазмы мускулатуры, анорексия, остеопороз.
Хроническая нехватка ионов Na+ и Cl- приводит к смерти. Биохимик Жорес Медведев отмечал, что при полном отсутствии в организме соли можно продержаться не больше 11 суток.
Племена скотоводов и охотников еще в древности для удовлетворения потребности организма в соли, употребляли в сыром виде мясопродукты. Земледельческие племена потребляли растительную пищу, в которой незначительное количество хлористого натрия. В качестве признаков, сигнализирующих о нехватке соли, выделяют слабость и головную боль, тошноту, головокружение.

Особенности производства
В далеком прошлом добыча соли осуществлялась путем сжигания в кострах определенных растений. Образующуюся золу применяли в виде приправы.
Очистка поваренной соли, полученной путем выпаривания морской воды, не проводилась, полученное вещество сразу же употреблялось в пищу. Такая технология возникла в странах с жарким и сухим климатом, где подобный процесс происходил без вмешательства человека, а затем, когда его переняли иные страны, морская вода стала подогреваться искусственным путем.
На берегах Белого моря строились солеварни, в которых путем выпаривания и замораживания получали концентрированный рассол и пресную воду.

Природные месторождения
Среди мест, характеризующихся большими запасами поваренной соли, выделим:
- Артемовское месторождение, расположенное в Донецкой области. Здесь осуществляется добыча соли шахтовым способом;
- озеро Баскунчак, перевоз ведется по специально построенной железной дороге;
- калийные соли в большом количестве обнаружены в Верхнекамском месторождении, где шахтовым способом идет добыча этого полезного ископаемого;
- в Одесских лиманах велась добыча до 1931 года, в настоящее время месторождение не используется в промышленных объемах;
- в Сереговском месторождении проводится выпаривание рапы.
Соляная шахта
Биологические свойства поваренной соли сделали ее важным экономическим объектом. На 2006 год на российском рынке использовалось порядка 4,5 миллионов тонн данного минерала, причем 0,56 млн тонн шло на пищевые расходы, а оставшиеся 4 миллиона тонн уходили на нужды химической промышленности.

Физические характеристики
Рассмотрим некоторые свойства поваренной соли. Данное вещество достаточно хорошо растворяется в воде, причем на процесс влияет несколько факторов:
- температура;
- наличие примесей.
Кристалл поваренной соли содержит примеси в виде катионов кальция, магния. Именно поэтому хлорид натрия впитывает воду (сыреет на воздухе). Если такие ионы не входят в состав поваренной соли, такое свойство отсутствует.
Температура плавления поваренной соли — 800,8 °С, что свидетельствует о прочной кристаллической структуры данного соединения. При смешивании мелкого порошка хлорида натрия с измельченным льдом получают охладитель высокого качества.
Например, 100 г льда и 30 г поваренной соли могут снижать температуру до −20 °C. Причина подобного явления в том, что раствор поваренной соли замерзает при температуре ниже 0 °C. Лед, для которого это значение является температурой плавления, плавится в подобном растворе, поглощая тепло окружающей среды.
Высокая температура плавления поваренной соли объясняет ее термодинамические характеристики, а также высокую диэлектрическую проницаемость – 6,3.

Получение
Учитывая, насколько важны биологические и химические свойства поваренной соли, ее существенные природные запасы, нет необходимости разрабатывать вариант промышленного производства данного вещества. Остановимся на лабораторных вариантах получения хлорида натрия:
- Данное соединение можно получить в качестве продукта при взаимодействии сульфата меди (2) с хлоридом бария. После удаления осадка, в качестве которого выступает сульфат бария, выпаривания фильтрата, можно получить кристаллы поваренной соли.
- При экзотермическом соединении натрия с газообразным хлором также образуется хлористый натрий, причем процесс сопровождается выделением существенного количества тепла (экзотермический вид).
Взаимодействия
Каковы химические свойства поваренной соли? Данное соединение образовано сильным основанием и сильной кислотой, поэтому гидролиз в водном растворе не протекает. Нейтральность среды и объясняет применение поваренной соли в пищевой промышленности.
При электролизе водного раствора данного соединения на катоде выделяется газообразный водород, а на аноде идет процесс образования хлора. В межэлектродном пространстве накапливается гидроксид натрия.
Учитывая, что получаемая щелочь – вещество, востребованное в различных производственных процессах, это также объясняет применение поваренной соли в промышленных масштабах на химическом производстве.
Плотность поваренной соли составляет 2,17 г/см3. Кубическая гранецентрированная кристаллическая решетка характерна для многих минералов. Внутри ее преобладают ионные химические связи, образуемые за счет действия сил электростатического притяжения и отталкивания.

Галит
Так как плотность поваренной соли в этом соединении достаточно высока (2,1—2, 2 г/см³), галит – твердый минерал. Процентное содержание катиона натрия в нем составляет 39,34 %, аниона хлора – 60, 66%. Помимо этих ионов, в составе галита есть в виде примесей ионы брома, меди, серебра, кальция, кислорода, свинца, калия, марганца, азота, водорода. Этот прозрачный бесцветный минерал, имеющий стеклянный блеск, образуется в замкнутых водоемах. Галит является продуктом сгона на кратерах вулканов.
Каменная соль
Он представляет собой горную осадочную породу из группы эвапоритов, которая состоит более чем на 90 процентов из галита. Для каменной соли характернее белоснежный цвет, лишь в исключительных случаях присутствие глины дает минералу серый оттенок, а наличие оксидов железа придает соединению желтый, оранжевый цвет. В каменной соли присутствует не только хлорид натрия, но и множество иных химических соединений магния, кальция, калия:
- иодиды;
- бораты;
- бромиды;
- сульфаты.
В зависимости от условий формирования, основные месторождения каменной соли подразделяют на несколько видов:
- подземные соляные воды;
- рассолы современных бассейнов;
- залежи минеральных солей;
- ископаемые месторождения.
Морская соль
Она является смесью сульфатов, карбонатов, хлоридов калия и натрия. В процессе ее испарения при диапазоне температур от +20 до +35 °C первоначально происходит кристаллизация менее растворимых солей: карбонатов магния и кальция, а также сульфата кальция. Далее в осадок выпадают растворимые хлориды, а также сульфаты магния и натрия. Последовательность кристаллизации этих неорганических солей может меняться с учетом температурного показателя, скорости процесса испарения, иных условий.
В промышленных объемах морская соль получается из воды морей путем выпаривания. Она существенно отличается по микробиологическим и химическим показателям от каменной соли, имеет большое процентное содержание йода, магния, калия, марганца. Из-за различного химического состава есть отличия и в органолептических показателях. Применяют морскую соль в медицине в качестве средства при лечении кожных заболеваний, например, псориаза. Среди распространенных продуктов, предлагаемых в аптечной сети, выделим соль Мертвого моря. Также морская соль в очищенном виде предлагается и в пищевой промышленности как йодированная.
Обычная поваренная соль имеет слабые антисептические свойства. При процентном содержании данного вещества в диапазоне 10-15 процентов можно предотвратить появление гнилостных бактерий. Именно для этих целей хлорид натрия добавляют в виде консерванта к пище, а также иным органических массам: древесине, клею, коже.

Злоупотребление солью
По информации Всемирной организации здравоохранения, избыточное потребление хлорида натрия приводит к существенному повышению кровяного давления, в результате чего нередко развиваются болезни почек и сердца, желудка, формируется остеопороз.
Вместе с другими солями натрия хлорид натрия является причиной появления заболеваний глаз. Поваренная соль задерживает внутри организма жидкость, что приводит к повышению внутриглазного давления, формированию катаракты.
Вместо заключения
Хлорид натрия, называемый в повседневной жизни поваренной солью, является широко распространенным в природе неорганическим минералом. Этот факт существенно упрощает его применение в пищевой, химической промышленности. Нет необходимости тратить временные и энергетические ресурсы на промышленное получение данного вещества, что сказывается на его стоимости. Для того чтобы не допускать переизбытка данного соединения в организме, необходимо контролировать ежедневное употребление соленых продуктов.
Молекулы соли: flavorchemist — LiveJournal
Бактерии являются причиной ожирения.
Показалось интересно, но не было отсылки на оригинальный источник, лишь ссылка на кулинарный портал. На котором нам предлагают узнать «Всю правду о соли»
Мелкая соль класса «Экстра» – это продукт термической и химической обработки. Такая соль не только теряет свою первоначальную структуру и все полезные свойства, но и обладает канцерогенными свойствами и является причиной повышения артериального давления. Перед тем, как попасть на наш стол, соль высушивается в огромных печах при температуре свыше 650°С! При такой сумасшедшей температуре молекулы соли просто лопаются и меняют свою структуру (КАК???). Затем в соль добавляют химические испарители влаги, чтобы соль была сухой и не слипалась в неаппетитный комок. Вместо природных солей йода, которые удаляются в процессе обработки, в соль добавляется йодид калия, который может быть токсичным, если его «переесть»
(спасибо clavinessa за картинку)
В итоге соль становится чужеродной нашему телу.
Согласно теории кислотно-щелочного баланса, почти все хронические болезни – это результат закисления крови, лимфы и всех тканей нашего организма. А настоящая морская соль является одним из щелочных элементов, необходимых нашему организму.
Морская соль содержит почти всю таблицу Менделеева, кроме газов (а как же хлор?), а это 84 элемента, и около 200 химических соединений! Состав кристалла морской соли настолько сложен, что человек до сих пор не сумел его создать искусственно.
Ну там еще много чего интересного. Может быть об этом говорил Баранов?
Дорогая Лариса Шуфтайкина, автор сего опуса. Продолжайте писать про рецепты, но не более того. Прежде чем писать про «лопающиеся молекулы», повторите школьную программу по химии.
Пошел дальше искать про бактерии и ожирение.
Соли: классификация и химические свойства
Солями называются сложные вещества, молекулы которых, состоят из атомов металлов и кислотных остатков (иногда могут содержать водород). Например, NaCl – хлорид натрия, СаSO4 – сульфат кальция и т. д.
 Практически все соли являются ионными соединениями, поэтому в солях между собой связаны ионы кислотных остатков и ионы металла:
Практически все соли являются ионными соединениями, поэтому в солях между собой связаны ионы кислотных остатков и ионы металла:
Na+Cl– – хлорид натрия
Ca2+SO42– – сульфат кальция и т.д.
Соль является продуктом частичного или полного замещения металлом атомов водорода кислоты. Отсюда различают следующие виды солей:
1. Средние соли – все атомы водорода в кислоте замещены металлом: Na2CO3, KNO3 и т.д.
2. Кислые соли – не все атомы водорода в кислоте замещены металлом. Разумеется, кислые соли могут образовывать только двух- или многоосновные кислоты. Одноосновные кислоты кислых солей давать не могут: NaHCO
3. Двойные соли – атомы водорода двух- или многоосновной кислоты замещены не одним металлом, а двумя различными: NaKCO3, KAl(SO4)2 и т.д.
4. Соли основные можно рассматривать как продукты неполного, или частичного, замещения гидроксильных групп оснований кислотными остатками: Аl(OH)SO4 , Zn(OH)Cl и т.д.
По международной номенклатуре название соли каждой кислоты происходит от латинского названия элемента. Например, соли серной кислоты называются сульфатами: СаSO
В название солей двухосновных кислот добавляют частицу «би» или «гидро»: Mg(HCl3)2 – бикарбонат или гидрокарбонат магния.
При условии, что в трехосновной кислоте замещён на металл только один атом водорода, то добавляют приставку «дигидро»: NaH2PO4 – дигидрофосфат натрия.
Соли – это твёрдые вещества, обладающие самой различной растворимостью в воде.

Химические свойства солей определяются свойствами катионов и анионов, которые входят в их состав.
1. Некоторые соли разлагаются при прокаливании:
CaCO3 = CaO + CO2↑
2. Взаимодействуют с кислотами с образованием новой соли и новой кислоты. Для осуществление этой реакции необходимо, чтобы кислота была более сильная чем соль, на которую воздействует кислота:
2NaCl + H2 SO4 → Na2SO4 + 2HCl↑.
3. Взаимодействуют с основаниями, образуя новую соль и новое основание:
Ba(OH)2 + Mg SO4 → BaSO4↓ + Mg(OH)2.
4. Взаимодействуют друг с другом с образованием новых солей:
NaCl + AgNO3 → AgCl + NaNO3 .
5. Взаимодействуют с металлами, которые стоят в раду активности до металла, который входит в состав соли:
Fe + CuSO4 → FeSO4 + Cu↓.
Остались вопросы? Хотите знать больше о солях?
Чтобы получить помощь репетитора – зарегистрируйтесь.
Первый урок – бесплатно!
Зарегистрироваться
Кристаллы
Валерия Сирота
«Квантик» №1, 2019
Нужно признаться, что в 10-м номере «Квантика» за 2018 год я вас немножко обманула. Не всех, а только тех, кто слепил из пластилина молекулы поваренной соли (NaCl) и оксида железа (Fe2O3). Дело в том, что таких молекул нет. Соль не состоит из молекул!
Если «посмотреть» на неё в очень сильный электронный микроскоп (в обычный оптический такие мелкие детали не разглядеть), окажется, что вместо того, чтобы попарно разделиться на молекулы — каждому атому натрия свой атом хлора, — все атомы построены, как солдаты на плацу! Да ещё и не на плоскости, а в пространстве. На одинаковых расстояниях друг от друга чередуются Na — Cl — Na — Cl —… Если этот строй и слепился из молекул, уже не различить, где какая, и не понять, с каким атомом хлора мог быть сцеплен этот атом натрия: все соседние атомы Cl находятся от него на равных расстояниях.
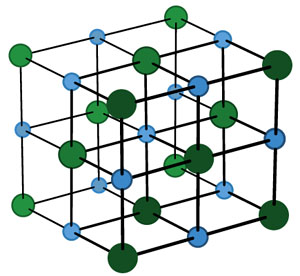
Это — ионный кристалл (рис. 1). Помните, что такое ионная связь? Атом хлора «отбирает» у атома натрия электрон, и оба атома становятся ионами — «дефектными» атомами с числом электронов, не равным числу протонов, и оттого заряженными: натрий положительным, а хлор отрицательным. Теперь они притягивают друг друга. Но если рядом много других таких же ионов, то ведь все отрицательные притягиваются ко всем положительным! Правда, от всех других отрицательных при этом отталкиваются. Получается, что им удобно расположиться в таком вот шахматном порядке. И хотя каждый отдельный хлор отобрал электрон у какого-то одного натрия, притягивается он ко всем своим соседям-натриям. Так что число связей-«ручек» оказывается намного больше.
Это соединение получается очень твёрдым и прочным. В магазинах в основном продают мелко помолотую соль, а если взять соль крупного помола или вообще «каменную» — необработанную, то раздробить её можно разве что молотком.
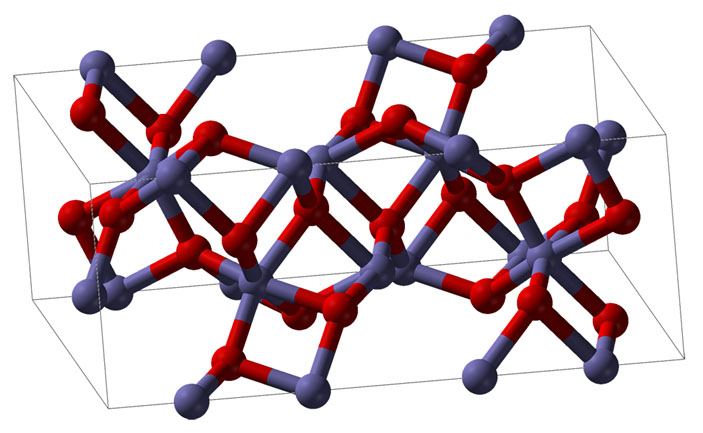
Оксид железа — тоже кристаллическое вещество, но ионы железа и кислорода выстраиваются иначе — кристаллическая решётка другая (рис. 2).
Кристаллы возникают не только у веществ с ионной связью между атомами. Они могут составляться и из таких атомов, которые делятся электронами друг с другом, а не отдают «насовсем» — это называется ковалентной связью. Так, углерод может образовывать даже несколько разных видов кристаллов, «под настроение» — смотря какие условия вокруг. И в зависимости от того, как построились атомы — одни и те же атомы углерода! — получаются совсем разные вещества. (А если атомы никак не построились, а «валяются» как попало — получается сажа.)
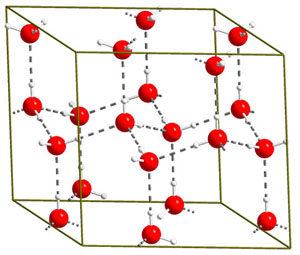
А бывает, что в кристаллы строятся не отдельные атомы, а целые молекулы. Например, лёд: это тоже кристаллическое вещество, но решётку образуют молекулы воды (рис. 4). В каждой молекуле воды кислород хоть и «делится» своими электронами с атомами водорода, но при этом «оттягивает» все общие электроны от ядер водорода — поближе к себе. Так что каждый электрон вроде бы вертится вокруг обоих ядер, но вокруг кислорода — больше. Получается, что кислород немножко заряжен отрицательно, а водород — положительно. И вот в результате кислородный «конец» одной молекулы притягивается к водородному «концу» другой. Это притяжение и удерживает их в решётке.
Но совсем особый вид связи, который бывает только в кристалле, придумали себе металлы. Это такие атомы, у которых по одному-два электрона на внешнем уровне-этаже, и им их отдать вовсе не жалко. Такие атомы «делятся» своими электронами не просто с ближайшим соседом, а со всеми остальными атомами кристалла! То есть все эти «лишние» электроны становятся общими и летают по всему кристаллу. А ионы — ядра с оставшимися электронами — стоят «в строю» и образуют кристаллическую решётку.
Большая свобода электронов обеспечивает одно из главных свойств металлов — способность проводить электрический ток. Ток — это упорядоченное (дружное, в одну сторону) движение заряженных частиц. Если присоединить кусок металла к батарейке, ионы решётки стоят неподвижно, а электроны бегут (точнее, дрейфуют — бегая туда-сюда, постепенно сдвигаются) все в одну сторону, к «плюсу» батарейки. Это не значит, что их в металле становится меньше: ведь ток течёт, только когда металлический провод подсоединён к батарейке. И вместо электронов, «убегающих» в батарейку на одном конце провода, из батарейки приходят новые электроны на другой конец. Провод при этом всегда остаётся незаряженным. Но если батарейку присоединить к куску пластмассы, резины или даже к сухой деревяшке — ток не потечёт: нет свободных электронов, все привязаны к своим молекулам, некому бежать.
Ещё металлы хорошо проводят тепло: попробуешь нагреть один конец — нагревается весь кусок металла. Это тоже из-за свободных электронов: летая между холодным и горячим концами, они переносят тепло и уравнивают температуру.
Кристаллическое или аморфное?
Вообще-то все «по-настоящему твёрдые» вещества, хорошо сохраняющие свою форму, — кристаллические. Хотя вот пластилин или глина например, когда засохнут, — вполне твёрдые, а вовсе не имеют кристаллической структуры. Такие вещества называются
У кристаллических веществ есть определённая температура плавления, у каждого своя; если нагреть их до этой температуры, они резко меняют свои свойства и плавятся, превращаются в жидкость: кристалл разваливается на отдельные молекулы. У аморфных тел никакой определённой температуры плавления нет — при нагревании они плавно становятся всё более текучими. Молекулы (или атомы) в них и так уже расположены как в жидкости.
Элементарная ячейка и виды решёток
Мы говорили в № 10 «Квантика» за 2018 год, что молекула — «минимальный кусочек» вещества, который ещё определяет его химические свойства: взяв много таких кусочков, получим сколько угодно этого вещества. У кристаллического вещества «минимальное количество», которое его всё ещё полностью определяет, — не молекула, а элементарная ячейка. Это самый маленький кусочек решётки, из копий которого можно составить всю решётку.
Например, кристаллическая решётка поваренной соли получается многократным повторением такого кусочка: Na — Cl. Это и есть элементарная ячейка соли, в ней два атома. А в элементарной ячейке полония — всего один атом (рис. 5). Такая кристаллическая решётка называется простой кубической: весь кристалл можно составить из одинаковых кубиков, в каждом — один атом (на рисунке один из этих кубиков выделен синим). Это и есть элементарная ячейка.
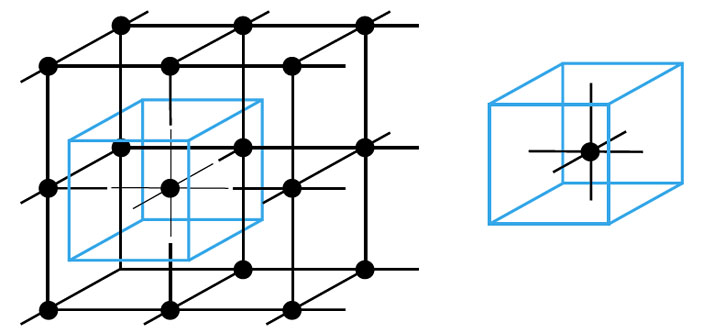
Обратите внимание! Чёрные линии, которыми на этом и следующих рисунках изображены связи между ионами, тоже образуют кубики. Но «разрезать» (даже мысленно) кристалл на ячейки удобнее не по ним — а то атомы попадут на границы разрезов, и мы легко запутаемся, разбираясь, «считается» ли этот атом внутри того или этого кубика. Лучше просто сдвинуть нашу воображаемую (синюю) сетку из элементарных ячеек.
Следующий по сложности тип решётки — такой, в котором атомы расположены не только по вершинам кубиков, нарисованных чёрными палочками-связями, но и в центре каждого кубика (рис. 6, слева). Так устроены, например, кристаллы железа. А другие атомы — например, меди и золота — предпочитают строиться в гранецентрированные решётки, у которых атомы стоят в вершинах кубов и в центрах их граней (рис. 6, справа).

Как мы видели на примере углерода, бывают и некубические решётки: у графита, например, элементарная ячейка имеет форму шестиугольной призмы.
Художник Мария Усеинова
Или побольше, но у атомов с очень большим количеством электронов, так что на верхних этажах «электронного дома» до ядра уже очень далеко и внешние электроны держатся совсем непрочно. Из-за этого в нижних строках таблицы Менделеева почти все элементы — металлы.
Можете проверить это, нагревая один конец вилки или ложки над плитой или опуская их в горячую воду. Только не обожгитесь.
Имеются в виду «чистые» вещества, из одинаковых молекул. Смеси разных веществ (как воздух или дерево) мы сейчас не обсуждаем.
Самые маленькие — потому что две соседние элементарные ячейки, например, тоже можно копировать, и получится то же самое. Интересно найти самый маленький из всех возможных «кирпичиков». Но всё-таки такой, который «сохраняет симметрии решётки»: если вся решётка симметрична, например переходит сама в себя при повороте на 90°, то и элементарная ячейка должна быть так же симметрична. В частности, если решётка состоит из кубов, то и элементарная ячейка должна иметь форму куба.
Гималайская соль под микроскопом
40 кратное увеличение. Гималайская и поваренная соль под микроскопом. Хорошо различима структура соли. Слева гималайская, справа поваренная соль.
100 кратное увеличение. Более детальное сравнение структуры гималайской и поваренной соли. Слева гималайская, справа поваренная соль.
400 кратное увеличение. Гималайская и поваренная соли под максимальным 400 кратным увеличением. Слева гималайская, справа поваренная соль.
Сравнение гималайской и поваренной солей под микроскопом
Фотографии гималайской соли с использованием микроскопа, появились в книге доктора Барбары Гендель «Вода и соль» и были сделаны доктором Хоефером (Dr. Hoefer). На фотографиях представлено сравнение структуры гималайской и поваренной соли при 400 кратном увеличении. Фотографии интересны тем что показывают четкую разницу между солями. Как различные биоэнергетические структуры влияют на усвоение человеческим организмом или на здоровье в целом по-прежнему остается загадкой и явно нуждается в дальнейшем исследовании. Здесь мы просто показываем разницу структур разных солей.
Если посмотреть в микроскоп на поваренную соль вы увидите не связанные и отдельные кристаллические структуры, отсоединённые друг от друга. Утверждается что многие жизненно важные минералы, которые может содержать соль не могут быть усвоены нашим организмом или организм расходует огромную энергию чтобы переваривать и усваивать их.
Гималайская соль является сбалансированной она не изолирована от других присутствующих в ней минеральных элементов, а соединяется с ними в гармоничном состоянии. Это означает что содержащиеся элементы могут легко метаболизироваться в организме. Используя гималайскую соль, мы получаем большую энергетическую ценность не затрачивая энергии на усвоение. Обусловлено это структурой гималайской соли, которая в свою очередь результат воздействия высочайшего давления на протяжении миллионов лет. Такое давление на протяжении невероятно долгого времени довело структуру гималайской соли до коллоидного состояния — в таком состоянии клетки организма легко усваивают любой продукт — в нашем случае это чистейшая гималайская соль.
Видео сравнение морской соли и гималайской
Структура гималайской соли
Доктор Гендель утверждает, что под электронным микроскопом гималайская соль имеет совершенную кристаллическую структуру. Поваренная соль сильно отличается по своей структуре. Для того чтобы ваше тело попыталась метаболизировать поваренную соль оно должно принести в жертву огромное количество энергии. Элементы в гималайской соли образуют соединение, в котором каждая молекула взаимосвязана. Она также утверждает, что все неотъемлемые минералы кристаллической соли и микроэлементы доступны в коллоидной форме — это означает что они настолько малы что человеческие клетки могут легко поглотить их.
Выводы
В итоге из этих фотографий хорошо видно, что гималайская соль по своей структуре намного более мелкая и однородная в отличии от поваренной соли. Это объясняется коллоидным состоянием гималайской соли. В таком состоянии клетки организма усваивают соль без энергетических затрат. При усвоении поваренной соли организм затрачивает значительные энергетические ресурсы, плюс может затрачивать в 23 раза больше молекул воды для нейтрализации поваренной соли, что в свою очередь может приводить к обезвоживанию. Более подробно в статье польза гималайской соли.
правда и мифы о популярном «гаджете»
Вы что-нибудь слышали о соляных лампах? Готовы спорить, что да. Говорят, что эти внушительные кристаллы соли с заботливо высеченным в центре отверстием, куда помещается лампа накаливания, способны превратить спальню в спа-курорт.
Если верить рекламе, соляные лампы могут очищать воздух, насыщать мозг кислородом, снимать симптомы расстройств настроения (в частности, сезонного аффективного расстройства) и укреплять иммунную систему. Что на этот счет думают ученые — в нашем материале.
Что говорят производители
По словам представителей Solay Wellness Inc. (компании, которая продает такие лампы), главным преимуществом «гаджетов» является то, что они производят отрицательные ионы.
«Соленый кристалл, естественно, гигроскопичен, то есть поглощает молекулы воды из воздуха. Вы заметите, что если ваша соляная лампа остается без подсветки в течение длительных периодов времени, она начинает «плакать». Тепло от небольшой лампочки держит кристаллы сухими и, в свою очередь, выпускает отрицательные ионы в воздух», — говорится в пресс-релизе.
Согласно DrAxe.com, кристаллы притягивают токсины и другие загрязняющие вещества к поверхности каменной соли, поскольку молекулы воды в воздухе могут переносить в себе грязь, плесень и аллергены. Все это звучит заманчиво, но проблема проста — ни одно из утверждений, которые можно обнаружить на сайтах производителей, не имеет научных обоснований и какого-либо смысла с точки зрения химии.
Что говорят ученые
Во-первых, если гималайская розовая, черная, морская и любая другая соль не особенно отличается по составу от обычной поваренной соли (об этом как раз говорят исследования), то преобладающими ионами, которые станут образоваться в результате работы соляной лампы, будут ионы натрия и хлорида. «Но соль стабильна, потому когда вы немного нагреваете ее, ничего не происходит», — говорит Live Science Джон Малин (John Malin), в прошлом член Американского химического общества (American Chemical Society).
Небольшое количество водяного пара в воздухе, конечно, может прилипать к поверхности соли, так что часть его способна диссоциировать соль в ионы натрия и хлорида. Но как только водяной пар высушивается, два типа ионов немедленно рекомбинируют И процесс вряд ли приведет к образованию отрицательных ионов.
Что касается очищения воздуха, то в этом тоже мало смысла. Некотор
Типы кристаллических решёток — урок. Химия, 8–9 класс.
Большинство твёрдых веществ имеет кристаллическое строение, которое характеризуется строго определённым расположением частиц.
Если соединить частицы условными линиями, то получится пространственный каркас, называемый кристаллической решёткой.
Точки, в которых размещены частицы кристалла, называют узлами решётки. В узлах воображаемой решётки могут находиться атомы, ионы или молекулы.
В зависимости от природы частиц, расположенных в узлах, и характера связи между ними различают четыре типа кристаллических решёток: ионную, металлическую, атомную и молекулярную.
Ионными называют решётки, в узлах которых находятся ионы.
Их образуют вещества с ионной связью. В узлах такой решётки располагаются положительные и отрицательные ионы, связанные между собой электростатическим взаимодействием.
Ионные кристаллические решётки имеют соли, щёлочи, оксиды активных металлов.
Ионы могут быть простые или сложные. Например, в узлах кристаллической решётки хлорида натрия находятся простые ионы натрия Na+ и хлора Cl−, а в узлах решётки сульфата калия чередуются простые ионы калия K+ и сложные сульфат-ионы SO42−.
Связи между ионами в таких кристаллах прочные. Поэтому ионные вещества твёрдые, тугоплавкие, нелетучие. Такие вещества хорошо растворяются в воде.

Кристаллическая решётка хлорида натрия
Кристалл хлорида натрия
Металлическими называют решётки, которые состоят из положительных ионов и атомов металла и свободных электронов.
Их образуют вещества с металлической связью. В узлах металлической решётки находятся атомы и ионы (то атомы, то ионы, в которые легко превращаются атомы, отдавая свои внешние электроны в общее пользование).
Такие кристаллические решётки характерны для простых веществ металлов и сплавов.
Температуры плавления металлов могут быть разными (от \(–37\) °С у ртути до двух-трёх тысяч градусов). Но все металлы имеют характерный металлический блеск, ковкость, пластичность, хорошо проводят электрический ток и тепло.
Металлическая кристаллическая решётка

Металлические изделия
Атомными называют кристаллические решётки, в узлах которых находятся отдельные атомы, соединённые ковалентными связями.
Такой тип решётки имеет алмаз — одно из аллотропных видоизменений углерода. К веществам с атомной кристаллической решёткой относятся графит, кремний, бор и германий, а также сложные вещества, например, карборунд SiC и кремнезём, кварц, горный хрусталь, песок, в состав которых входит оксид кремния(\(IV\)) SiO2.
Таким веществам характерны высокая прочность и твёрдость. Так, алмаз является самым твёрдым природным веществом.
У веществ с атомной кристаллической решёткой очень высокие температуры плавления и кипения. Например, температура плавления кремнезёма — \(1728\) °С, а у графита она выше — \(4000\) °С.
Атомные кристаллы практически нерастворимы.

Кристаллическая решётка алмаза

Алмаз
Молекулярными называют решётки, в узлах которых находятся молекулы, связанные слабым межмолекулярным взаимодействием.
Несмотря на то, что внутри молекул атомы соединены очень прочными ковалентными связями, между самими молекулами действуют слабые силы межмолекулярного притяжения. Поэтому молекулярные кристаллы имеют небольшую прочность и твёрдость, низкие температуры плавления и кипения.
Многие молекулярные вещества при комнатной температуре представляют собой жидкости и газы.
Такие вещества летучи. Например, кристаллические иод и твёрдый оксид углерода(\(IV\)) («сухой лёд») испаряются, не переходя в жидкое состояние.
Некоторые молекулярные вещества имеют запах.
Такой тип решётки имеют простые вещества в твёрдом агрегатном состоянии: благородные газы с одноатомными молекулами (He,Ne,Ar,Kr,Xe,Rn), а также неметаллы с двух- и многоатомными молекулами (h3,O2,N2,Cl2,I2,O3,P4,S8).
Молекулярную кристаллическую решётку имеют также вещества с ковалентными полярными связями: вода — лёд, твёрдые аммиак, кислоты, оксиды большинства неметаллов. Большинство органических соединений тоже представляют собой молекулярные кристаллы (нафталин, сахар, глюкоза).

Кристаллическая решётка углекислого газа

«Сухой лёд»
Кристаллики иода
Если известно строение вещества, то можно предсказать его свойства.
Попробуем определить, каковы примерно температуры плавления у фторида натрия, фтороводорода и фтора.
У фторида натрия — ионная кристаллическая решётка. Значит, его температура плавления будет высокой. Фтороводород и фтор имеют молекулярные кристаллические решётки. Поэтому их температуры плавления будут невысокими. Молекулы фтороводорода полярные, а фтора — неполярные. Значит, межмолекулярное взаимодействие у фтороводорода будет сильнее, и его температура плавления будет выше по сравнению со фтором.
Экспериментальные данные подтверждают эти предположения: температуры плавления NaF, HF и F2 составляют соответственно \(995\) °С, \(–83\) °С, \(–220\) °С.
Источники:
Габриелян О. С. Химия. 8 класс. Учебник для общеобразовательных учреждений. М.: Дрофа, 2013. — 133 с.

Leave a Reply